Fonctions des protéines : exemple du transport de l’oxygène
1. Introduction : place du transport de l’oxygène dans les processus biologiques
La création d’énergie disponible pour les processus biologiques est le premier impératif du vivant.
On extrait 18 fois plus d’énergie à partir du glucose en présence qu’en absence d’oxygène.
Chez les vertébrés, deux protéines sont capables de fixer l’oxygène :
- La myoglobine est une protéine simple et fixe l’oxygène avec une forte affinité.
- L’hémoglobine est une protéine complexe et fixe l’oxygène avec une affinité modulable.
2. Myoglobine
2.1. La myoglobine a une structure compacte et riche en hélice alpha
Protéine de 153 résidus :
- de forme globulaire (« sphérique »)
- de 45x35x25 Å
- monomérique
- riche en hélices α
Représentations de la structure 3D de la myoglobine de cachalot par diffraction X :
| Schéma simplifié | Modèle en cylindre | Modèle à haute résolution |
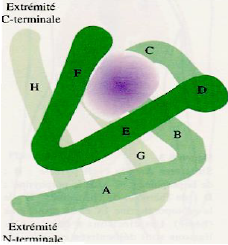 | 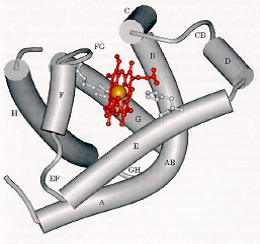 | 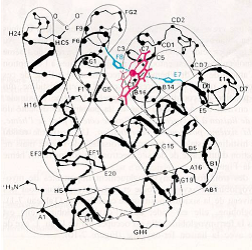 |
2.2. L’oxygène est fixé sur la myoglobine grâce à l’hème, un groupement prosthétique
La myoglobine est constituée de 2 parties :
- Apoprotéine = partie protéique dépourvue de groupement prosthétique
- Hème = groupement prosthétique = molécule non peptidique mais nécessaire à la fonction
L’hème est constitué d’un noyau protoporphirine IX et du fer. Cette molécule est
- cyclique, plane et polaire
- constituée de 4 unités de base : cycle pyrrole.
| Unité de base : cycle pyrrole | Hème |
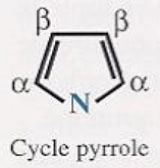 | 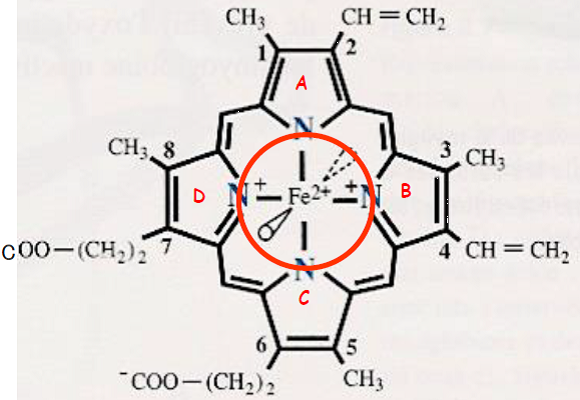 |
Le fer joue un rôle majeur dans cette fixation.
Le fer est sous forme ferreuse Fe2+ (ferromyoglobine) et dispose de 6 liaisons de coordination dont 4 avec l’hème.
L’oxydation du fer en forme ferrique Fe3+ (ferrimyoglobine) rend la molécule inactive.
Dans le cas de l’hémoglobine, ces formes s’appellent respectivement ferrohémoglobine (Fe2+) et ferrihémoglobine ou methémoglobine (Fe3+).
2.3. La liaison de l’hème à la myoglobine dépend principalement de deux résidus histidine
| Sans O2 2 liaisons de coordination entre Fe2+ et 2 histidines de la myoglobine : une histidine proximale et une distale | Avec O2 L’oxygène s’intercale entre l’histidine distale et Fe2+ avec lequel se forme une liaison de coordination. La liaison avec l’histidine proximale est maintenue. La fixation d’oxygène déplace l’atome de fer par rapport au plan de l’hème. => Déplacement de l’atome de fer dans le plan de l’hème et mouvement transmis à l’histidine proximale. |
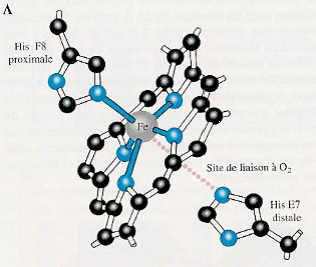 | 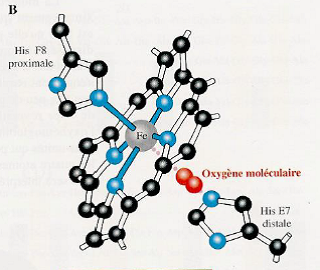 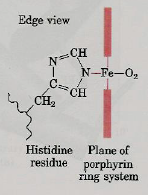 |
Le monoxyde de carbone CO se lie au fer de façon compétitive avec l’O2 avec une affinité beaucoup plus forte. Il bloque le chargement et le transport de l’O2, d’où son effet toxique.
2.4. La liaison de l’oxygène à la myoglobine suit une courbe hyperbolique
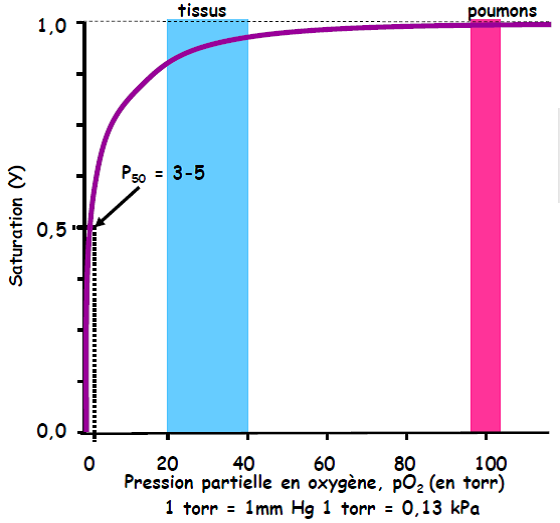
La courbe hyperbolique traduit la très haute affinité de la myoglobine pour l’oxygène.
La myoglobine n’est pas adaptée pour le transport et la libération de l’oxygène dans les tissus.
3. Hémoglobine
3.1. L’hémoglobine est composée de 4 sous-unités de structure proche de celle de la myoglobine
| Myoglobine | Chaîne β de l’hémoglobine |
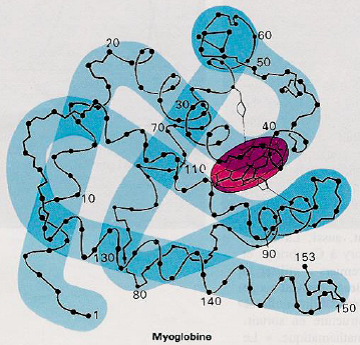 | 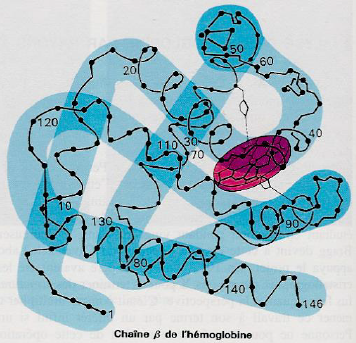 |
3.2. L’hémoglobine adulte contient 2 chaînes alpha et deux chaînes bêta. Cette structure confère à la molécule des caractéristiques de protéine allostérique
Protéine allostérique :
- comporte généralement plusieurs sous-unités,
- possède plusieurs sites de liaisons pour un/des ligands
- et telle que la liaison d’un ligand sur un site modifie la liaison des autres ligands.
Molécule d’hémoglobine tétramérique avec 2 chaînes alpha et 2 chaînes bêta maintenues par des interactions non covalentes (liaisons ioniques ou ponts salins).
Chaque chaîne possède un hème et un site de liaison de l’O2, soit fixation de 4 molécules d’O2 pour une molécule Hb.
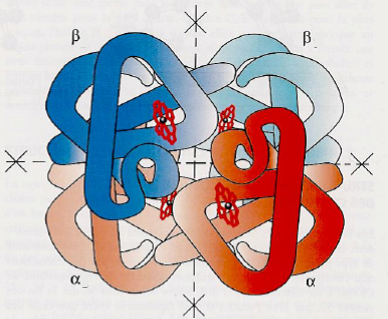
L’évolution de la myoglobine vers l’hémoglobine confère à cette dernière des propriétés remarquables :
- coopérativité de la liaison de l’O2 : la fixation des molécules d’oxygène facilite la fixation des molécules suivantes
- possibilité de modulation physiologique de la fixation de l’oxygène par : pH, CO2, DPG…
Remarque : on note l’hémoglobine adulte HbA α2β2. Il existe de nombreuses autres chaînes possibles pour l’hémoglobine, comme par exemple l’hémoglobine fœtale HbF α2γ2.
3.3. L’hémoglobine est parfaitement adaptée pour la captation, le transport et la libération de l’oxygène dans les tissus : modulations de l’affinité pour O2
L’affinité de Hb pour 02 est plus faible que celle de la myoglobine et est modulable. La courbe sigmoïde traduit l’effet coopératif.
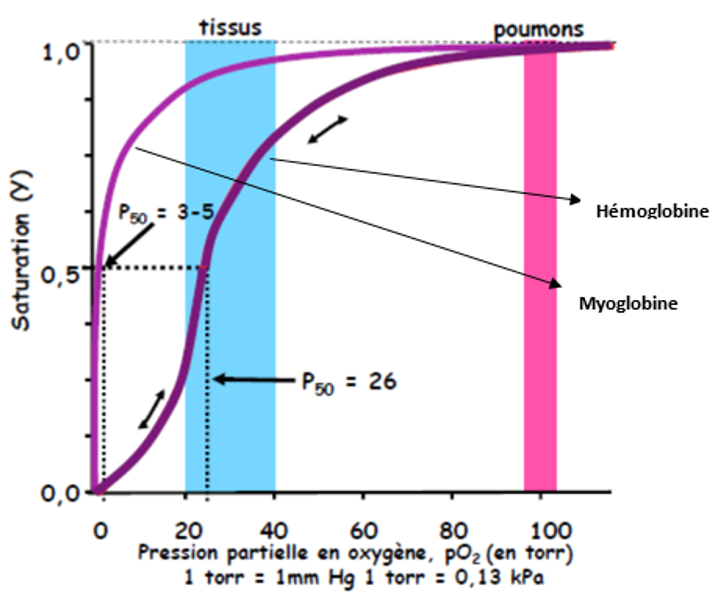
Fixation d’O2 : (sang = hémoglobine et muscles = myoglobine) visualisées par des courbes de saturation.
Courbes de saturation = % de protéine ayant fixé de l’O2 en fonction de la pression partielle en oxygène pO2
Détermination de la P50 = pression de l’oxygène pour laquelle la saturation est de 50 %
=> Plus la P50 est élevée, plus l’affinité pour l’oxygène est faible et donc plus la libération d’oxygène est élevée.
| Pour la myoglobine | Courbe de saturation hyperbolique. P50 faible donc forte affinité, non modulable et donc pas allostérique. La myoglobine permet de stocker l’oxygène dans le muscle. |
| Pour l’hémoglobine | Courbe de saturation sigmoïde = effet coopératif dans la fixation de l’O2 . La fixation d’une molécule d’O2 facilite la fixation de la molécule suivante d’O2. La P50 est plus élevée que pour la myoglobine. Seule l’hémoglobine peut transporter et libérer l’O2 dans les tissus. |
Modulation de l’affinité :
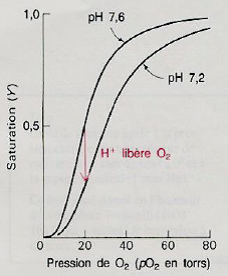
1)L’affinité de l’hémoglobine pour O2 est diminuée par la diminution du pH (augmentation de [H+])
2)L’affinité de Hb pour O2 est diminuée par l’augmentation de CO2.
=> Effet BOHR
| pH | pO2 | pCO2 | ||
| Poumons | 7.4 | 100 torrs | 100% | |
| Muscles | 7.4 | 20 torrs | 66 % capacité libérée | |
| Muscles | 7.2 | 20 torrs | 77 % de capacité libérée | |
| Muscles | 7.2 | 20 torrs | 40 torrs | 90 % de capacité libérée |
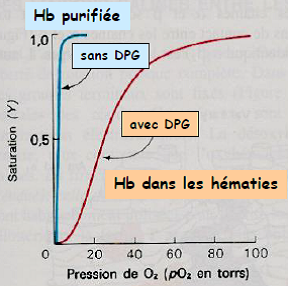
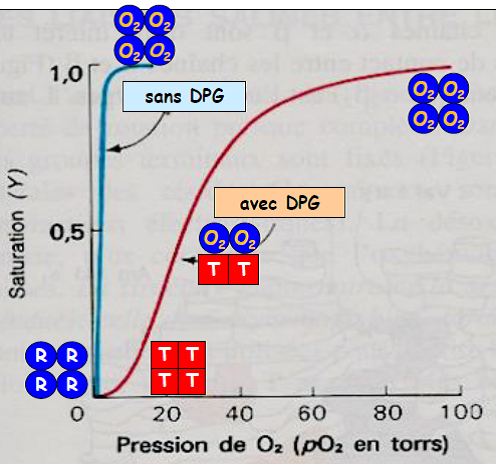
3)L’affinité de Hb pour O2 est diminuée par le 2,3 diphospho-glycérate (DPG).
Le DPG est :
- un intermédiaire de la glycolyse,
- libéré dans les tissus périphériques
- et présent dans les hématies à la même concentration que l’hémoglobine (2 mM).
En absence de DPG, l’hémoglobine perd ses propriétés de coopérativité, et son comportement est similaire à celui de la myoglobine.
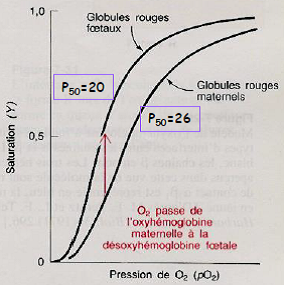
L’affinité de l’hémoglobine fœtale (HbF = α2γ2) pour O2 est supérieure à celle de l’hémoglobine maternelle (HbA = α2β2).
Cette différence d’affinité HbF > HbA est liée à la plus faible affinité de la chaîne γ de HbF pour le DPG comparée à la chaîne b de HbA.
3.4. L’analyse tridimensionnelle de l’hémoglobine permet de définir le mécanisme moléculaire de son fonctionnement
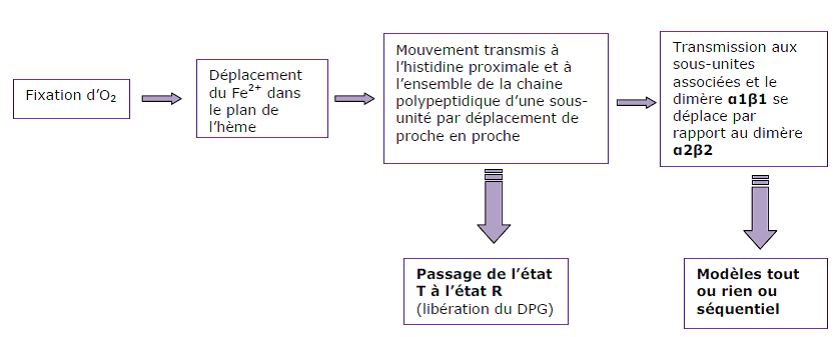
Lors de l’oxygénation, l’atome de fer se déplace vers le plan de l’hème.
Ce mouvement est transmis à l’histidine proximale et à l’ensemble de la chaîne polypeptidique par déplacement de proche en proche.
- Trait noir : en l’absence d’O2
- Trait bleu : après fixation d’O2
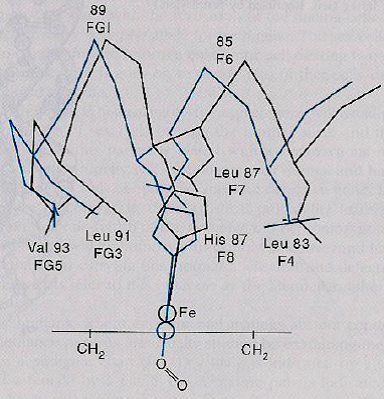
Les déplacements générés sur une sous-unité sont transmis à une sous-unité associée.
Les interactions entre chaînes adjacentes sont principalement réalisées par des ponts salins entre résidus chargés.
Modèle à basse résolution indiquant les zones de contact α-β.
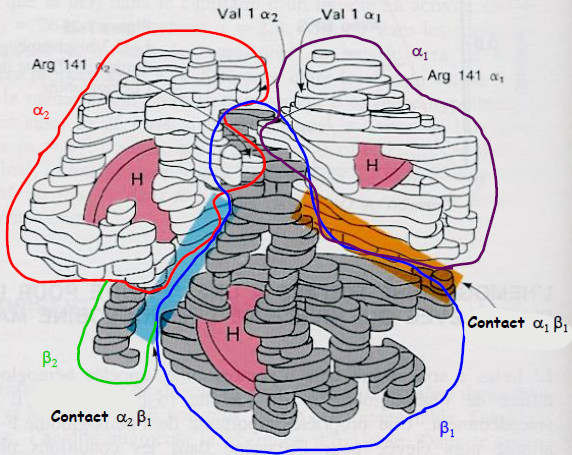
La résultante globale est un mouvement du dimère α1β1 par rapport à α2β2.
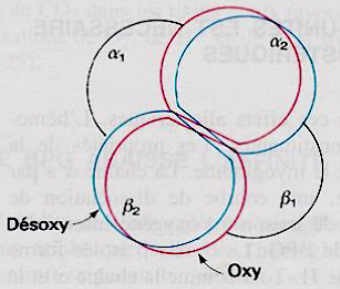
La comparaison des structures de l’oxyHb et de la désoxyHb indique l’existence de deux états moléculaires distincts.
| Etat relâché R a une forte affinité pour O2 | Etat tendu T a une faible affinité pour O2 |
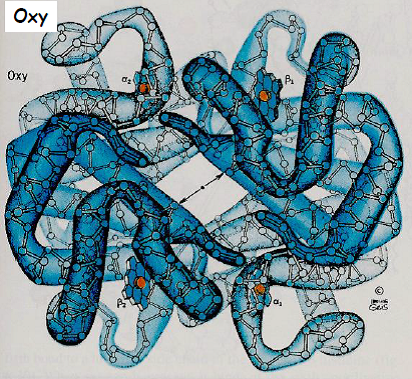 | 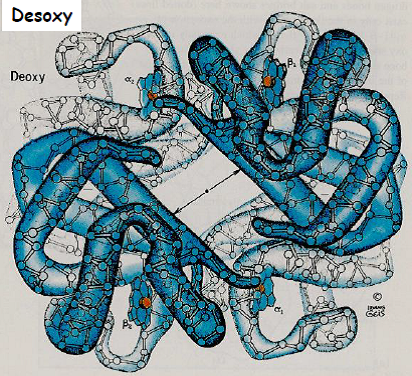 |
Le 2,3 DPG bloque l’hémoglobine en position T en se fixant dans l’espace libre entre les 4 sous-unités. C’est pourquoi il interfère avec la coopérativité.
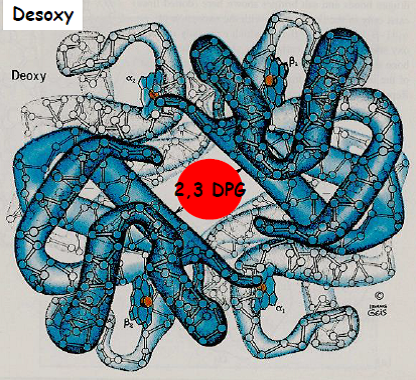
3.5. L’hémoglobine sert de modèle pour les protéines allostériques
Il existe deux modèles pour la «transition» allostérique de l’hémoglobine.
Considérons pour simplifier deux états de l’hémoglobine :
| Etat tendu T |  | – faible affinité pour O2 (Hb desoxygénée) – stabilisée par le DPG, le CO2 et les protons H+ |
| Etat relâché R | – forte affinité pour l’O2 (Hb oxygénée), sans DPG |
La « transition » allostérique peut suivre deux voies :
| Modèle du « tout ou rien » ou modèle symétrique | Les 4 sous-unités sont initialement toutes à l’état T et la présence d’O2 déplace l’équilibre vers l’état R. Les 4 sous-unités passent toutes à l’état R et fixent l’une après l’autre l’O2. 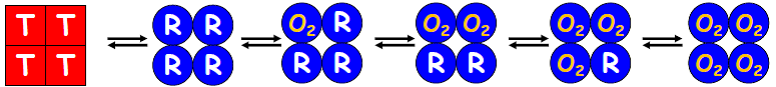 |
| Modèle séquentiel | Les 4 sous-unités sont initialement toutes à l’état T et passent au fur et à mesure à l’état R par fixation d’une molécule d’O2.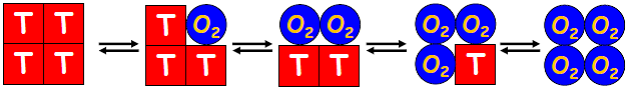 |
Sans DPG, la forme R est favorisée même en absence d’O2.
3.6. L’hémoglobine sert de modèle pour l’étude des pathologies moléculaires
L’exemple de la drépanocytose
- Hémoglobine S = HbS (sous-unité β mutée) provoque la drépanocytose : même fonction, même affinité, régulation et coopérativité que HbA.
- Lors du passage de l’OxyHbS à la désoxyHbS (libération de l’oxygène), changement de conformation favorisant l’apparition d’une poche hydrophobe due à la mutation ponctuelle qui fait apparaître un acide aminé hydrophobe : une valine.
- Cela entraine une polymérisation des sous-unités β des hémoglobines et la formation de polymères de désoxyHbS.
- Ces polymères anormaux déforment les hématies (hématies falciformes).
- Ces hématies anormales sont détruites entrainant la diminution du nombre de globules rouges.
Un autre exemple de situation pathologique : le monoxyde de carbone (CO) inhibe de manière compétitive, la fixation d’O2 sur l’hémoglobine ou la myoglobine en se fixant au site actif de l’hémoglobine ou la myoglobine.
