Etats d’équilibres acido-basique
Ce que vous savez du lycée
| De la seconde : | / |
| De la première : | / |
| De la terminale : | Les transformations acide-base sont caractérisées par des transferts d’ion hydrogène H+. Dans ce cadre, vous avez défini les notions d’acide et de base de Brönsted, de couple acide-base, de réaction acide-base et d’espèce amphotère. A titre d’exemples, vous avez décrit les couples acide-base de l’eau, de l’acide carbonique, d’acides carboxyliques, d’amines. Ainsi, vous savez : – identifier, à partir d’observations ou de données expérimentales, un transfert d’ion hydrogène, les couples acide-base mis en jeu et établir l’équation d’une réaction acide-base. – représenter le schéma de Lewis et la formule semi-développée d’un acide carboxylique, d’un ion carboxylate, d’une amine et d’un ion ammonium. – identifier le caractère amphotère d’une espèce chimique. Vous avez ensuite analysé un système chimique par des méthodes physiques et appris la notion de pH et la relation pH = – log ([H3O+] / c°) avec c° = 1 mol•L-1, concentration standard. Ainsi, vous savez : – déterminer, à partir de la valeur de la concentration en ion oxonium H3O+, la valeur du pH de la solution et inversement. – mesurer le pH de solutions d’acide chlorhydrique (H3O+, Cl–) obtenues par dilutions successives d’un facteur 10 pour tester la relation entre le pH et la concentration en ion oxonium H3O+ apporté. Capacité mathématique demandée : savoir utiliser la fonction logarithme décimal et sa réciproque. Dans une seconde partie de votre enseignement, vous avez appris à comparer la force des acides et des bases au travers de la constante d’acidité KA d’un couple acide-base, produit ionique de l’eau Ke. Ainsi, vous savez : – associer KA et Ke aux équations de réactions correspondantes. – estimer la valeur de la constante d’acidité d’un couple acide-base à l’aide d’une mesure de pH. Au travers de l’étude de la réaction d’un acide ou d’une base avec l’eau, ainsi que l’étude des cas limites des acides forts et des bases fortes dans l’eau, vous savez : – associer le caractère fort d’un acide (d’une base) à la transformation quasi-totale de cet acide (cette base) avec l’eau. – prévoir la composition finale d’une solution aqueuse de concentration donnée en acide fort ou faible apporté. – comparer la force de différents acides ou de différentes bases dans l’eau. – mesurer le pH de solutions d’acide ou de base de concentration donnée pour en déduire le caractère fort ou faible de l’acide ou de la base. – déterminer le taux d’avancement final d’une transformation, modélisée par la réaction d’un acide sur l’eau. Capacité mathématique demandée : savoir résoudre une équation du second degré. Vous avez également étudié les solutions courantes d’acides et de bases et vous savez citer des solutions aqueuses d’acides et de bases courantes et les formules des espèces dissoutes associées : acide chlorhydrique (H3O+(aq), Cl–(aq)), acide nitrique (H3O+(aq), NO3-(aq)), acide éthanoïque (CH3COOH(aq)), soude ou hydroxyde de sodium (Na+(aq), HO–(aq)), ammoniac (NH3(aq)). L’étude des notions de diagrammes de prédominance et de distribution d’un couple acide-base, d’espèce prédominante, des cas des indicateurs colorés et des acides alpha-aminés, vous permet de : – représenter le diagramme de prédominance d’un couple acide-base. – exploiter un diagramme de prédominance ou de distribution. – justifier le choix d’un indicateur coloré lors d’un titrage. – tracer le diagramme de distribution des espèces d’un couple acide-base de pKA donné. Pour finir, vous savez définir et citer les propriétés d’une solution tampon. |
1. Objectifs
- Savoir définir un acide, une base, une constante d’acidité
- Savoir déterminer la force des acides et des bases en milieu aqueux
- Savoir définir le pH et le déterminer pour un acide fort/faible ou une base forte/faible en milieu aqueux
- Solutions tampons
- Dosages acido-basiques
2. Définitions
2.1. Monoacide et monobase
| Acide de Brönsted (AH ou BH+) | espèce pouvant libérer un proton H+ pour le donner à une autre espèce. |
| Base de Brönsted (A– ou B) | espèce susceptible de capter un proton en provenance d’une autre espèce. |
Acide <=> Base + H+
L’acide et la base sont dits « conjugués » ; ils forment un couple noté : acide / base.
Exemple : CH3COOH <=> CH3COO– + H+
2.2. Polyacide et polybase
| Polyacide | espèce pouvant libérer 2 ou plusieurs protons. |
| Polybase | espèce pouvant fixer 2 ou plusieurs protons. |
Exemple du sulfure d’hydrogène : H2S <=> 2H+ + S2- H2S est un diacide capable de libérer deux protons. S2- est une dibase pouvant fixer deux ions H+.
2.3. Ampholyte
Un ampholyte est un composé qui peut se comporter comme un acide ou comme une base.
Les solutions correspondantes, c’est-à-dire celles composées d’ampholytes, sont qualifiées d’amphotères.
Exemple : Considérons les 2 couples acido-basiques suivants : H2S/HS– et HS–/S2-, l’ion HS– est un ampholyte, car il joue le rôle d’un acide dans le couple HS–/S2- et se comporte comme une base dans le couple H2S/HS–.
3. Réaction acido-basique en milieux aqueux
Une réaction acido-basique implique 2 couples Acide-Base conjugués qui échangent des H+
Couple 1 : Acide(1) / Base(1) : Acide(1) <=> Base(1) + H+
Couple 2 : Acide(2) / Base(2) : Base(2) + H+ <=> Acide(2)
Réaction acido-basique : Acide(1) + Base(2) <=> Base(1) + Acide(2)
L’eau est un ampholyte appartenant aux 2 couples suivants :
- couple 1 : H3O+ / H2O : H3O+ <=> H2O + H+ (l’eau fixe H+ : c’est une base)
- couple 2 : H2O / OH– : H2O <=> H+ + HO– (l’eau cède H+ : c’est un acide)
=> Le caractère ampholyte de l’eau se traduit alors par la superposition des réactions :
| Réaction « d’autoprotolyse » | H2O + H2O <=> H3O+ + HO– acide(1) + base(2) <=> base(1) + acide(2) |
Lorsqu’on introduit un acide (AH) ou une base (B) dans l’eau, il se produit alors une réaction entre la substance introduite et le solvant (eau) :
Exemples :
| CH3COOH + H2O <=> CH3COO– + H3O+ acide(1) + base(2) <=> base(1) + acide(2) | NH3 + H2O <=> NH4+ + OH– base(2) + acide(1) <=> acide(2) + base(1) |
3.1. Constante d’équilibre
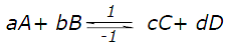
La constante d’équilibre K de toute réaction acido-basique est donnée par la loi d’action de masse :
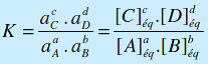
ΔrG°(T) = -RT LnK
où : aA, aB, aC et aD sont les activités des espèces A, B, C et D à l’équilibre et [A]éq, [B]éq, [C]éq et [D]éq les concentrations de ces mêmes espèces à l’équilibre
Equilibre de dissociation de l’eau
L’équilibre d’autoprotolyse de l’eau : 2 H2O <=> H3O+ + HO–est caractérisé par une constante d’équilibre Ke appelée « produit ionique » de l’eau.
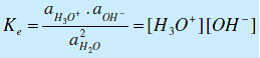
à 25°C : Ke= 10-14 d’où pKe = -log Ke = 14
ΔrG°(T) ≈ 80 kJ.mol-1
Variation de Ke avec la température : loi de van t’Hoff

3.2. Constante d’acidité Ka
Lorsqu’un acide faible AH est mis dans l’eau, il se produit une dissociation :
AH + H2O <=> A– + H3O+ (couple AH/A–)
acide(1) + base(2) <=> base(1) + acide(2)
La constante d’équilibre de dissociation de l’acide HA, ou « constante d’acidité » Ka, s’écrit :
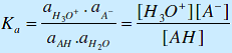
aH20 =1
On pose : pKa = – log Ka
3.3. Force des acides et des bases
Un acide est d’autant plus fort qu’il cède plus facilement un proton H+
AH + H2O <=> A– + H3O+
=> Plus un acide est fort, plus l’équilibre est déplacé dans le sens 1 et par conséquent plus Ka est grand : acidité croissante <=> Ka augmente ; pKa diminue
Une base est d’autant plus forte qu’elle capte plus facilement un proton H+
A– + H3O+ <=> AH + H2O
=> Plus une base est forte, plus l’équilibre est déplacé dans le sens 1 et par conséquent plus Ka est faible : basicité croissante <=> Ka diminue ; pKa augmente
L’eau est à la fois un acide et une base. Les pKa des 2 couples servant de référence sont :
- H3O+/H2O (Ka = 1 donc pKa = 0 à 25°C)
- H2O/HO– (Ka = 10-14 donc pKa = 14 à 25°C).
Exemples de couples acido-basiques
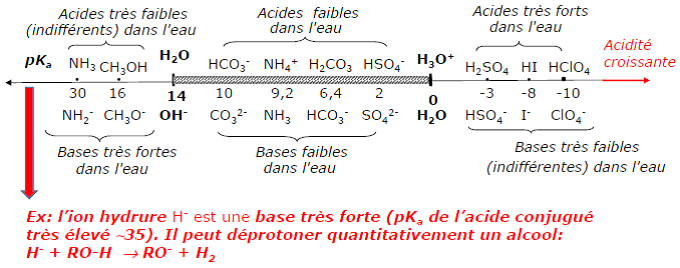
En comparant la force de l’acide AH d’un couple acido-basique AH/A–, on en déduit celle de sa base conjuguée A– par l’intermédiaire de la valeur du pKa.
- Pour un pKa négatif à 25°C, le couple acido-basique est composé d’un acide fort (AF) et d’une base très faible qu’on dit indifférente.
- Pour un pKa compris entre 0 et 14 à 25°C, le couple acido-basique est composé d’un acide faible (Af) et d’une base faible (Bf).
- Pour un pKa supérieur à 14 à 25°C, le couple acido-basique d’un acide très faible qu’on dit indifférent et d’une base forte (BF).
Remarque : Un acide indifférent est une entité qui n’a pas de potentiel acide et donc une base indifférente est une entité sans réel potentiel basique.
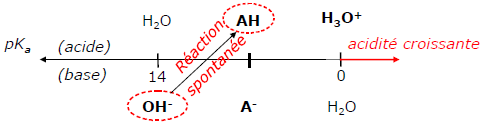
3.4. Sens d’évolution spontané des réactions AH/B
Considérons la réaction entre deux couples acido-basiques :
Acide(1) + Base(2) <=> Base(1) + Acide(2)
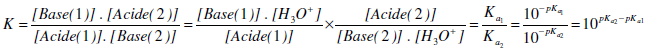
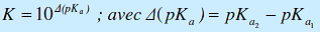
| Premier cas | Ka1 > Ka2 ou pKa2 > pKa1 : la constante de l’équilibre K est supérieure à 1. L’équilibre précédent est déplacé dans le sens 1. La réaction se fait donc entre la base la plus forte (pKa le plus grand) ET l’acide le plus fort (pKa la plus faible). 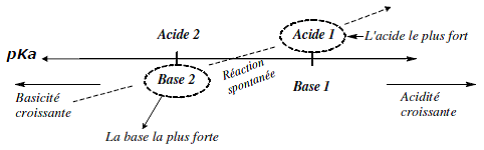 |
| Deuxième cas | Ka1 < Ka2 ou pKa2 < pKa1 : la constante de l’équilibre K est inférieure à 1. L’équilibre précédent est déplacé dans le sens -1. La réaction se fait donc entre la base la plus forte (pKa le plus grand : Base(1)) ET l’acide le plus fort (pKa la plus faible : Acide(2)) La réaction spontanée est dite quantitative ou totale lorsqu’elle consomme au moins 99 % du réactif limitant. C’est le cas pour K > 104 ou Δ(pKa) > 4. |
Exemple :
On considère les deux couples NH4+/NH3 et CH3COOH/CH3COO–.
La réaction acido-basique s’écrit : NH3 + CH3COOH <=> NH4+ + CH3COO–.
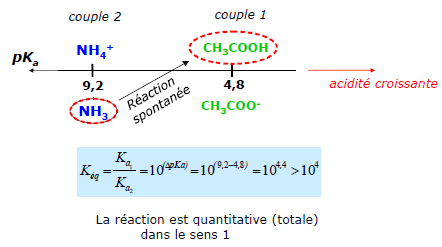
La réaction est quantitative (totale) dans le sens 1.
4. pH (potentiel d’hydrogène)
4.1. Définition du pH
L’acidité d’une solution aqueuse dépend de la concentration en ions H3O+
Le pH est tel que pH = -log [H3O+] (en solution diluée) dont la valeur est comprise entre 0 et pKe (14 à 25°C).
[H3O+] est exprimée en mol.L-1
4.2. Relation entre pH et pKa
Tout couple acide/base faible est caractérisé par sa constante d’acidité :
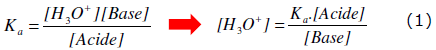
Sachant que : pH = -log [H3O+] et pKa = -log Ka
La relation (1) s’écrit :
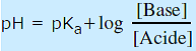
Relation d’Henderson
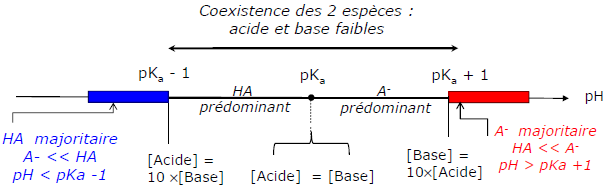
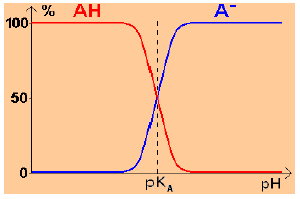
4.3. Diagramme de prédominance
Une espèce prédomine sur une autre quand sa concentration lui est supérieure.
Une espèce est majoritaire par rapport à une autre quand sa concentration lui est 10 fois supérieure.
- si pH = pKa, [Acide] = [Base]
- si pH > pKa, [Acide] < [Base] : la base est l’espèce prédominante
- si pH < pKa, [Acide] > [Base] : l’acide est l’espèce prédominante
Diagramme de prédominance : représentation graphique délimitant les domaines de concentration
4.4. Détermination du pH
Exemple du pH de l’eau
Soit l’équilibre d’autoprotolyse de l’eau : 2 H2O <=> H3O+ + OH– Ke = 10-14
On remarque que les quantités d’ions H3O+ et OH– sont stœchiométriques
D’où, dans l’eau pure, on a :
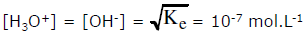
(Ke = [H3O+]×[OH–] = 10-14 à 25°C)
Le pH de l’eau pure sera : pH = – log [H3O+] = – log 10-7 = 7 = (pKe/2)
pH(eau) = 7
Les solutions neutres contiennent autant d’ions H3O+ que d’ions OH– :
[H3O+] = [OH–] => pH = pKe = 7 à 25°C
Les solutions acides contiennent plus d’ions H3O+ que d’ions OH– :
[H3O+] > [OH –] => pH < ½ pKe ; soit pH < 7 à 25°C
Les solutions basiques contiennent moins d’ions H3O+ que d’ions OH– :
[H3O+] < [OH –] => pH > ½ pKe ; soit pH > 7 à 25°C
Echelle de pH de l’eau
| Echelle de pH de l’eau pure à 25°C | 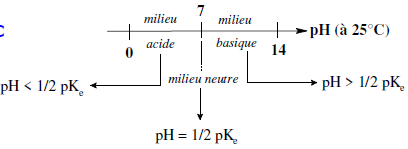 |
| Echelle de pH de l’eau pure à 50°C | 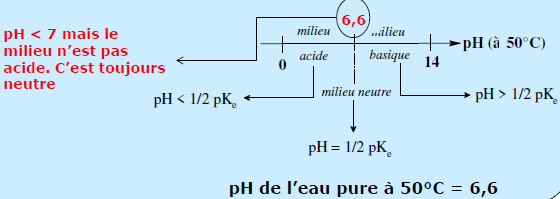 |
4.5. pH d’un monoacide fort
Lorsque l’on dissout dans l’eau un acide fort HA de concentration initiale Co, on a :
- Dissolution totale de l’acide : HA + H20 -> H3O+ + A–
à t = 0 Co 0 0
à t = équilibre 0 Co Co
- Autoprotolyse de l’eau : 2H20 <=> H3O+ + OH–
=> Dans le cas de solutions peu diluées (Co > 10-6,5 mol.L-1), le milieu est suffisamment acide pour que [OH–] et [H3O+] issus de l’autoprotolyse de l’eau soient négligeables devant [H3O+] issu de la dissociation de HA.
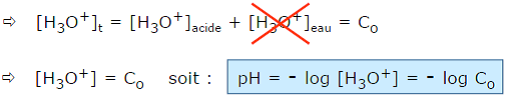
Validité de l’approximation : OH– négligeable devant H3O+
Une espèce telle que OH–, est considérée comme minoritaire et par conséquent sa concentration est négligeable devant celle de [H3O+] si :
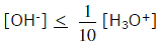
En multipliant les deux membres par [H3O+] :
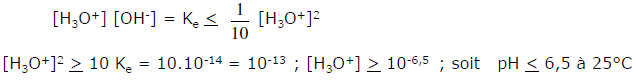
Donc la formule : pH = – log Co est valable jusqu’à un pH égal à 6,5
Exemple :

4.6. pH d’une monobase forte
Lorsque l’on dissout dans l’eau une base forte B de concentration initiale Co, on a :
- Protonation totale de la base : B + H20 -> BH+ + OH–
à t = 0 Co 0 0
à t = équilibre 0 Co Co
- Autoprotolyse de l’eau : 2H20 <=> H3O+ + OH–
=> Dans le cas de solutions peu diluées (Co > 10-6,5 mol.L-1), le milieu est suffisamment basique pour que [H3O+] issu de l’autoprotolyse de l’eau soient négligeable devant [HO–] issu de la dissociation de HA.
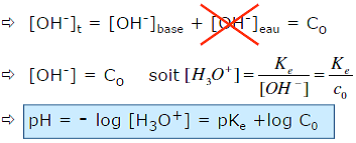
Validité de l’approximation : OH– négligeable devant H3O+
Une espèce telle que H3O+, est considérée comme minoritaire et par conséquent sa concentration est négligeable devant celle de [OH–] si :
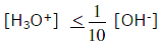
En multipliant les deux membres par [OH–] :
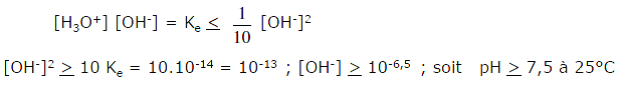
Donc la formule : pH = pke + log Co est valable pour un pH calculé supérieur à 7,5
Exemple : solution de soude NaOH de concentration initiale Co = 10-3 mol.L-1
pH = pKe + log Co = 14 + log 10-3 = 11
pH > 7,5
=> La formule est donc valide.
4.7. pH d’un monoacide faible
Soit une solution d’un monoacide faible HA de concentration initiale Co.
Deux équilibres se produisent simultanément :
- Dissociation de l’acide : HA + H2O <=> H3O+ + A–
- Autoprotolyse de l’eau : 2 H2O <=> H3O+ + OH–
4 espèces sont présentes à l’équilibre, en concentration : [HA], [A-], [H3O+] et [OH–]
On peut écrire quatre relations entre ces 4 inconnues :
| Produit ionique de l’eau | Ke = [H3O+] [OH–] | (1) |
| Constante d’acidité du couple HA/A– | (2) | |
| Conservation des éléments du couple acido-basique | Co = [HA] + [A–] | (3) |
| Electroneutralité de la solution | [H3O+] = [A–] + [OH–] | (4) |
Le calcul conduit à une équation du 3ème degré en [H3O+] :
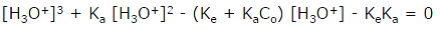
d’où la nécessité éventuelle de simplifier en faisant simultanément deux approximations.
| 1ère approximation : « le milieu est acide » : [H3O+] >> [OH–] | Pour un pH inférieur à 6,5 ([H3O+] ³ 3.10-7), [OH–] devient négligeable devant [H3O+]. Cette approximation dite « du milieu acide » est applicable sauf au voisinage immédiat de pH = 7. Cela revient à dire que l’acide apporte plus d’ions H3O+ que l’autoprotolyse de l’eau. L’équation (4) devient alors : 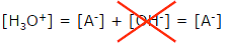 |
| 2ème approximation : « l’acide est faible » | La dissociation de l’acide est faible ; la concentration de la monobase conjuguée A– est négligeable devant celle de l’acide HA : [A–] << [HA]. L’équation (3) devient alors : 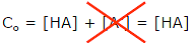 L’équation (2) devient alors : 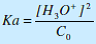 |
Validité de l’approximation : [A–] << [AH]
- On considère qu’un acide est faiblement dissocié si :

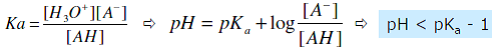
- On considère qu’un acide est faiblement dissocié si : α = coefficient de dissociation de AH = ξ/C0V < 0,1
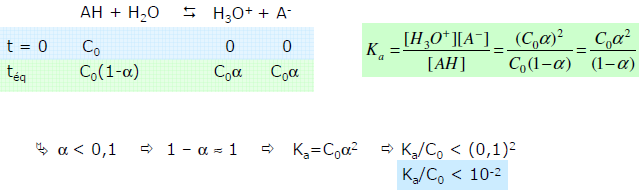
Récapitulatif
La formule qui donne le pH d’un monoacide faible dans l’eau :
pH = ½ (pKa – logC0)
est valable si [A–] << [AH]
- pH < pKa – 1
- Ka/C0 < 10-2
Et si par ailleurs le milieu est acide (autoprotolyse négligeable)
- pH < 6,5
Exemple : Calculer le pH d’une solution d’acide acétique CH3COOH (pKa = 4,8) de concentration Co = 10-1 mol.L-1 :
pH = ½ (4,8 + 1) = 2,9
La formule qui donne le pH est valide, puisque
- pH = 2,9 < 4,8 -1 = 3,8
- Ka/C0 = 10-4,8/10-1 = 10-3,8 < 10-2
- pH = 2,9 < 6,5
4.8. pH d’une monobase faible
Soit une solution d’une monobase faible B de concentration initiale Co.
Deux équilibres se produisent simultanément :
- Dissociation de l’acide : B + H2O <=> BH+ + OH– équivalent à B + H3O+ <=> BH+ + H2O
- Autoprotolyse de l’eau : 2 H2O <=> H3O+ + OH–
4 espèces sont présentes à l’équilibre, en concentration : [BH+], [B], [H3O+] et [OH–]
On peut écrire quatre relations entre ces 4 inconnues :
| Produit ionique de l’eau | Ke = [H3O+] [OH–] | (1) |
| Constante d’acidité du couple HA/A– | (2) | |
| Conservation des éléments du couple acido-basique | Co = [B] + [BH+] | (3) |
| Electroneutralité de la solution | [H3O+] + [BH+] = [OH–] | (4) |
Le calcul conduit à une équation du 3ème degré en [H3O+] :
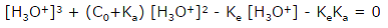
d’où la nécessité éventuelle de simplifier en faisant simultanément deux approximations.
| 1ère approximation : « le milieu est basique » : [H3O+] << [OH–] | Pour un pH supérieur à 7,5, [H3O+] devient négligeable devant [OH–]. Cette approximation dite « du milieu basique » est applicable sauf au voisinage immédiat de pH = 7. Cela revient à dire que la base apporte plus d’ions OH– que l’autoprotolyse de l’eau. L’équation (4) devient alors : 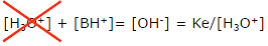 |
| 2ème approximation : « la base est faible » | La protonation de la base est faible ; la concentration de la monoacide conjuguée BH+- est négligeable devant celle de l’acide B : [BH+] << [B]. L’équation (3) devient alors : 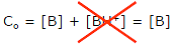 L’équation (2) devient alors : 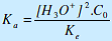 |
Validité de l’approximation : [BH+] << [B]
- On considère qu’une base est faiblement protonée si :

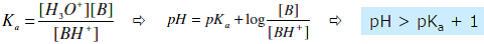
- On considère qu’une base est faiblement protonée si : α = coefficient de protonation de B = ξ/C0V < 0,1
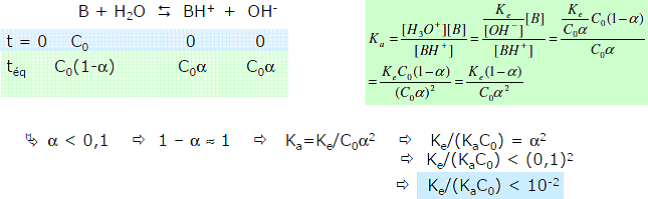
Récapitulatif
La formule qui donne le pH d’une monobase faible dans l’eau :
pH = ½ (pKa +pKe – logC0)
est valable si [BH+] << [B]
- pH > pKa + 1
- Ke/(KaC0) < 10-2
Et si par ailleurs le milieu est basique (autoprotolyse négligeable)
- pH > 7,5
Exemple : Calculer le pH d’une solution d’ammoniaque NH3 (pKa = 9,2) de concentration Co = 10-2 mol.L-1 :
pH = ½ (9,2 + 14 – 2) = 10,6
La formule qui donne le pH est valide, puisque
- pH > 9,2 + 1 = 10,2
- Ke/(KaC0) = 10-14/(10-9,2. 10-2) = 10-2,8 < 10-2
- pH = 10,6 > 7,5
4.9. pH d’une solution ampholyte
Soit HA– un ampholyte : il est l’acide du couple HA–/A2– et la base du couple H2A/HA–.
Deux réactions faisant intervenir HA- se produisent :
Base du couple H2A/HA– HA– + H3O+ <=> H2A + H2O Ka1-1
Acide du couple HA–/A2– HA– + H2O <=> A2– + H3O+ Ka2
Bilan 2 HA– <=> H2A + A2-
Le bilan de cette réaction globale indique que : [H2A] = [A2-]
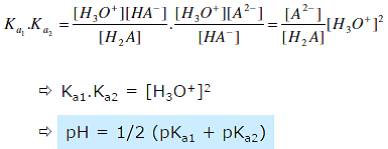
4.10.pH de solutions salines : exemples
| pH d’une solution d’un sel d’acide fort et de base forte | NaCl (chlorure de sodium) issu de la réaction de HCl et NaOH En solution aqueuse, il y a dissolution totale du sel : – Cl– : base conjuguée (très faible) d’un acide fort (HCl) – Cl– est un ion indifférent ou spectateur (ne participe à aucun équilibre acido-basique) – Na+ : ion spectateur, acide conjugué (très faible) d’une base forte (NaOH) => pH (NaCl) = pH (eau pure) = ½ (pKe) = 7 à 25°C |
| pH d’une solution d’un sel d’acide fort et de base faible | NH4Cl (chlorure d’ammonium) issu de la réaction de HCl et NH3 En solution aqueuse, il y a dissolution totale du sel : – Cl– : base conjuguée (très faible) d’un acide fort (HCl) – NH4+ : acide conjugué (faible) de la base faible NH3 (pKa = 9,2) => pH (NH4Cl) = pH (NH4+) => pH d’un acide faible => pH = ½ (pKa – log[NH4+]) (sous réserve que pH < pKa – 1, Ka/C0 < 10-2, pH < 6,5) |
| pH d’une solution d’un sel d’acide faible et de base forte | CH3COONa (acétate de sodium) issu de la réaction de CH3COOH et NaOH En solution aqueuse, il y a dissolution totale du sel : – Na+ : ion spectateur, acide conjugué (très faible) d’une base forte (NaOH) – CH3COO– : base conjuguée (faible) de l’acide faible CH3COOH (pKa = 4,8) => pH (CH3COONa) = pH (CH3COO-) => pH d’une base faible => pH = ½ (pKe + pKa + log[CH3COO–]) (sous réserve que pH > pKa + 1, Ke/(KaC0) < 10-2, pH > 7,5) |
| pH d’une solution d’un sel d’acide faible et de base faible | CH3COONH4 (acétate d’ammonium) issu de la réaction de CH3COOH et NH3 En solution aqueuse, il y a dissolution totale du sel : Mélange d’une base faible et d’un acide faible On va montrer que pH = 1/2 (pKa1 + pKa2) 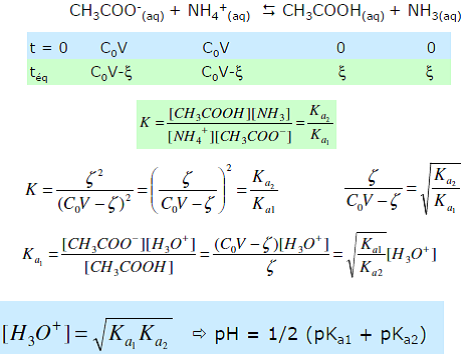 |
5. Solutions tampons
Une solution tampon
- est constituée d’un acide faible et de sa base conjuguée ou inversement (d’une base faible et son acide conjugué).
- minimise les variations de pH provoquées par une addition modérée d’acide ou de base ou par addition modérée d’eau (dilution).
Les solutions tampons sont particulièrement importantes dans les systèmes biologiques.
- Le sang et les autres fluides cellulaires sont tamponnés à pH ≈ 7,4.
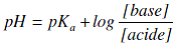
Si [acide]= [base] : pH = pKa => solution tampon d’efficacité maximale pour le couple.
D’une façon générale, on suppose que pour qu’une solution contenant les formes de l’acide AH et de sa base conjuguée A– exerce un effet tampon, il faut qu’il existe au moins 10 % de la base A– ou de l’acide AH, soit :
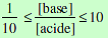
Il faut avoir un pH compris entre pKa – 1 et pKa + 1 :
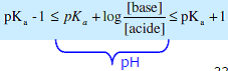
Solution tampon = mélange d’un acide faible AH et de sa base conjuguée A– dans des proportions égales ou voisines (couple AH/A–).
- Exemple : AH + sel NaA (solide)
En général le pH d’une solution tampon est compris entre 4 < pH (solution tampon) < 10
[H3O+] et [OH–] < 10-4 mol·L-1
Pour des raisons d’efficacité tampon, les concentrations C1 de l’acide faible AH et C2 du sel NaA sont relativement élevées c’est-à-dire > 10-2 mol.L-1 donc > à [H3O+] et [OH–].
Etant donné que [H3O+] et [OH–] sont négligeables devant [AH] et [NaA], on peut écrire :
C1 = [AH] => AH : acide faible, peu dissocié dans l’eau
C2 = [A–] => NaA : sel entièrement dissous dans l’eau
Le pH devient alors :
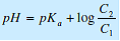
relation d’Henderson
Exemple : solution tampon réalisée à l’aide d’une mélange de NH3 (C1) et NH4+ (C2) avec C1 = C2 = 10-1 mol.L-1
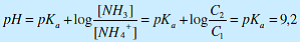
On rajoute dans 1 L de ce tampon, n1 moles de NaOH (base forte) avec : nNaOH = 10-2 mol.
Quel est le nouveau pH ? (on suppose que le volume reste égal à 1 L après ajout de NaOH).
L’ajout de NaOH provoque la réaction totale :
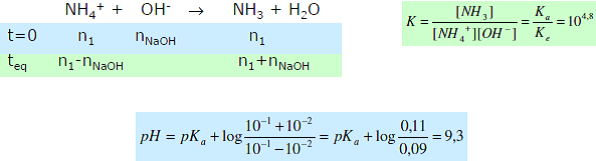
6. Dosages acido-basiques
6.1. Dosage d’un monoacide fort par une monobase forte
Soit HCl et NaOH mis en solution aqueuse.
Les ions Cl– et Na+ étant indifférents, la réaction globale qui se produit est donc :
H3O+ + OH– –> 2H2O K = (Ke)-1 = 1014
K > 104, on peut donc considérer que la réaction est totale (quantitative).
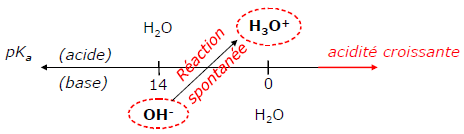
L’étude d’une réaction de dosage acide-base consiste en général à suivre l’évolution du pH de la solution en fonction du volume V2 de réactif ajouté (ou du nombre de moles n2 = C2V2)

L’équivalence acido-basique est l’état du mélange réactionnel obtenu quand les réactifs, introduits dans l’état initial selon les proportions stœchiométriques, sont totalement consommés.
α acide1 + β base2 –> γ base2 + δ acide2
A l’équivalence β.n1 = α.n2 => β.C1V1 = α.C2V2
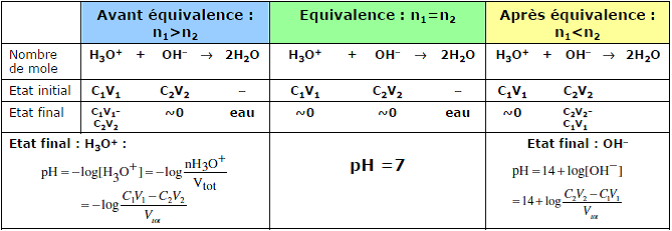
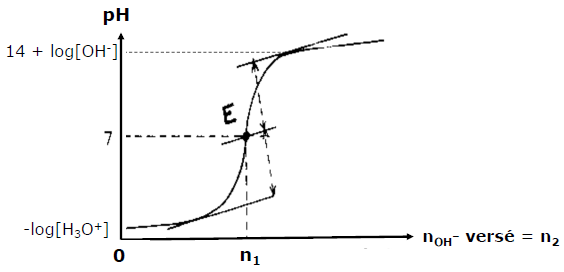
Allure du graphe pH = f(nOH- versé)
6.2. Dosage d’un monoacide faible par une monobase forte
HA + OH– –> A– + H2O K = Ka/Ke = 10(14-pKa)
Si pKa < 10, 10(14-pKa) > 104, on peut donc considérer que la réaction est totale (quantitative).
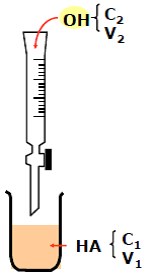
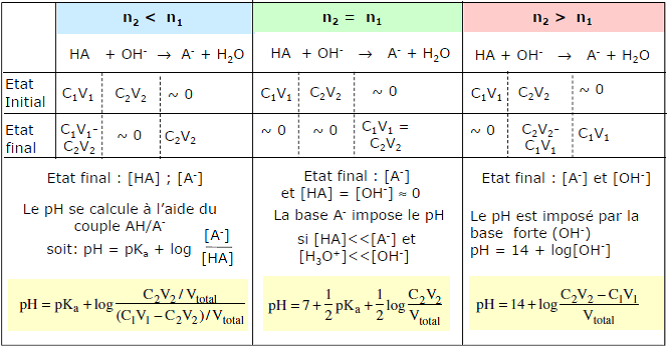
Cas particulier : demi-équivalence n2 = n1 / 2
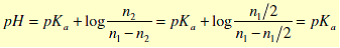
pH1/2eq = pKa, c’est un mélange tampon avec une efficacité maximale
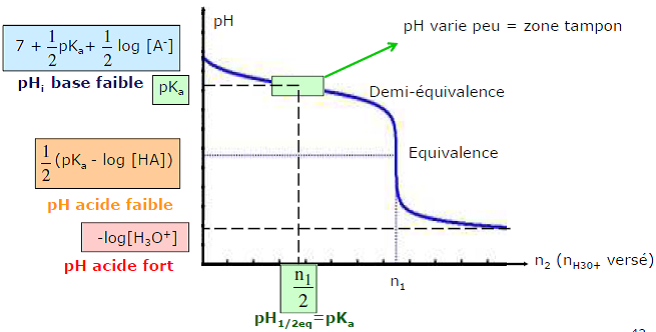
Allure du graphe pH = f(nOH- versé)
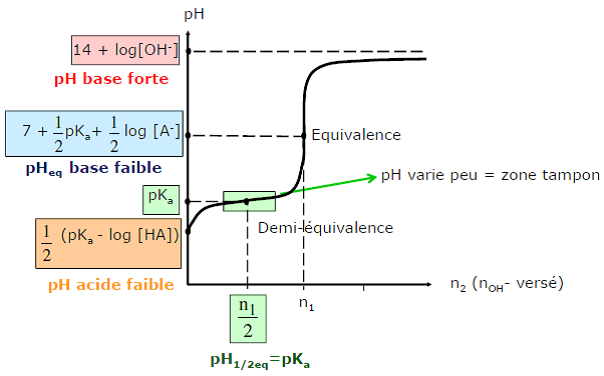
6.3. Dosage d’une monobase faible par un monoacide fort
A– + H3O+ –> AH + H2O K = 1/Ka = 10pKa
Allure du graphe pH = f(nH3O+ versé)