Stratégies pour l’étude des protéines
Ce que vous savez du lycée
| De la seconde : | / |
| De la première : | / |
| De la terminale : | / |
1. Isoler la/les protéine(s) responsable(s) d’une fonction
Exemple : on s’intéresse à la chymotrypsine, enzyme pancréatique sécrétée dans le tube digestif, responsable d’une étape de digestion des protéines alimentaires.
On dispose d’une méthode de mesure de l’activité de l’enzyme qui va permettre de suivre l’ensemble du processus.
Les étapes à suivre seront :
- isoler le tissu pancréatique ou collecter les sécrétions
- isoler l’organite (ici, Réticulum Endoplasmique Rugueux – RER) par centrifugations différentielles
- extraire les protéines totales
- séparer les protéines par chromatographie et électrophorèse
- isoler et purifier l’enzyme par affinité
- découper la protéine en petites unités (peptides)
- analyser la composition chimique des peptides (acides aminés)
- déterminer la séquence de la protéine entière
- étudier la structure 3D de la protéine
- déduire son mécanisme d’action
2. Isoler l’organite par centrifugations différentielles
Au départ, on dispose d’un homogénat cellulaire.
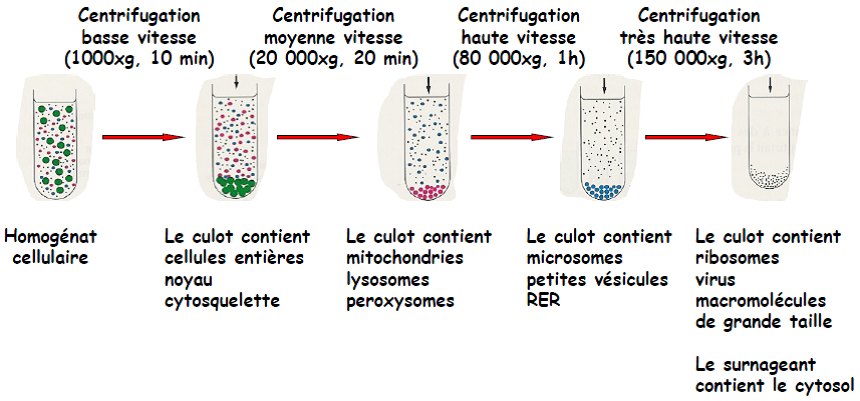
| Paramètres de la centrifugation | Basse vitesse | Moyenne vitesse | Haute vitesse | Très haute vitesse |
| Vitesse (g) | 1 000 | 20 000 | 80 000 | 150 000 |
| Temps (min) | 10 | 20 | 60 | 180 |
| Contenu du culot | Cellules entières Noyau Cytosquelette | Mitochondries Lysosomes Peroxysomes | Microsomes (= fragments de membranes) Petites vésicules RER | Virus Ribosomes Molécules de grande taille Remarque : le surnageant contient le cytosol |
3. Extraire les protéines totales
Différentes techniques d’isolement spécifiques d’organites ou de protéines peuvent être utilisées.
Extraction : extraire les protéines totales à partir d’une fraction subcellulaire purifiée. L’extraction des protéines totales repose sur leurs propriétés d’insolubilité dans des solutions salines.
4. Séparer les protéines par chromatographie et électrophorèse
4.1. Chromatographie
Séparer les protéines par chromatographie à travers leur migration différentielle à travers un système composé de deux phases : une phase fixe et une phase mobile.
On peut ainsi séparer les protéines en utilisant leurs différences :
- de taille,
- de charge,
- d’absorption spécifique.
Colonne de chromatographie comportant les deux phases
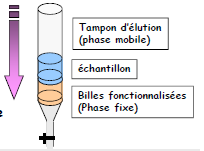
Les trois grands types de chromatographie utilisés pour purifier les protéines
| Séparation selon la charge | Séparation selon la taille | Séparation par absorption spécifique |
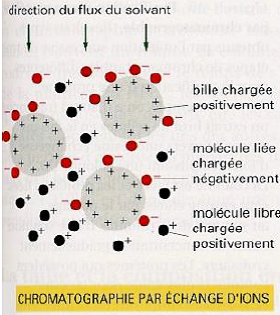 | 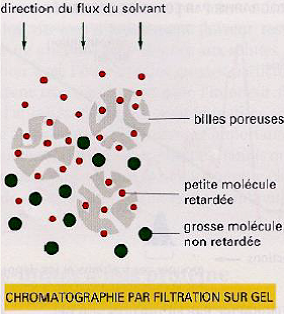 | 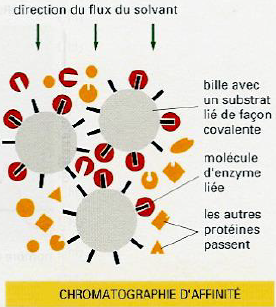 |
| Les billes sont chargés + ou – Elution par force ionique croissante | Les billes sont poreuses Séparation selon le poids ou la masse moléculaire Les grandes protéines font peu de chemin dans la colonne et sont élués en 1er alors que les petites protéines passent dans les billes et sont éluées en dernier. | Billes couplées à un ligand La protéine se lie à son ligand (anticorps ou enzyme) |
Rappel de la fiche 1 : Une protéine porte des charges positives et négatives au niveau des chaînes latérales des résidus d’acides aminés. Ces charges dépendent du pH de la solution et leur somme algébrique définit la charge globale de la protéine. Il existe toujours un pH pour lequel le nombre de charges positives portées par une protéine est égale au nombre de charges négatives ; la charge globale est alors nulle. Ce pH s’appelle le point isoélectrique de la protéine (pI). C’est la base de la séparation des protéines par électrofocalisation (voir également électrophorèse bi dimensionnelle).
4.2. Electrophorèse mono-dimensionnelle (SDS-PAGE)
Séparation des protéines selon leur masse moléculaire
Les plus petites migrent le plus vite et le plus loin car elles sont moins freinées par le gel. Elles migrent vers l’anode (pôle -)
Pourquoi SDS-PAGE ?
- SDS = Sodium Dodécyl Sufate = agent dénaturant anionique (-) qui rompt les liaisons faibles et charge la protéine négativement.
- PAGE = électrophorèse en gel de polyacrylamide : migration des protéines à travers un gel grâce à un champ électrique.
Une protéine peut être formée par plusieurs sous-unités (protéine multimérique) à l’aide de liaisons faibles ou de pont disulfures (S-S).
- Les liaisons faibles (non covalentes) sont rompues par le SDS. La structure tridimensionnelle est ainsi perdue.
- Les ponts disulfures (liaisons covalentes) sont rompus par le β-mercapto-éthanol.
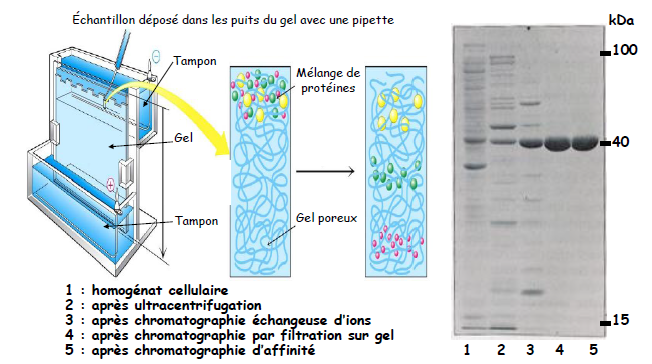
Remarque : Le Dalton Da est l’unité de masse. La masse d’un Dalton correspond à la masse d’un atome d’hydrogène.
4.3. Electrophorèse Bi-dimensionnelle
Permet de voir, séparer et analyser TOUTES les protéines d’une cellule
Séparation des protéines selon :
- leur pI ou leur charge globale grâce à un gradient de pH
- et leur taille
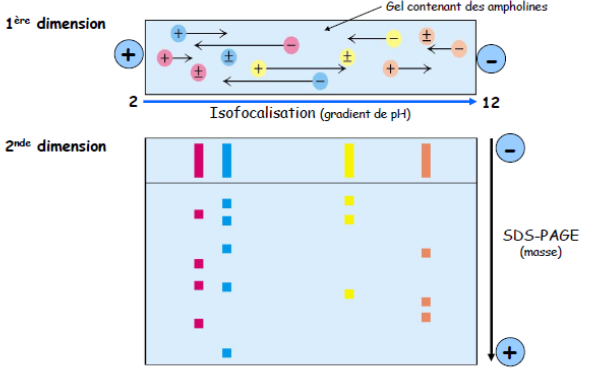
Première dimension (selon la charge) : électrofocalisation (= isofocalisation) en conditions non dénaturantes (sans SDS, ni β-mercapto-éthanol).
Seconde dimension (selon la taille) : électrophorèse SDS-PAGE
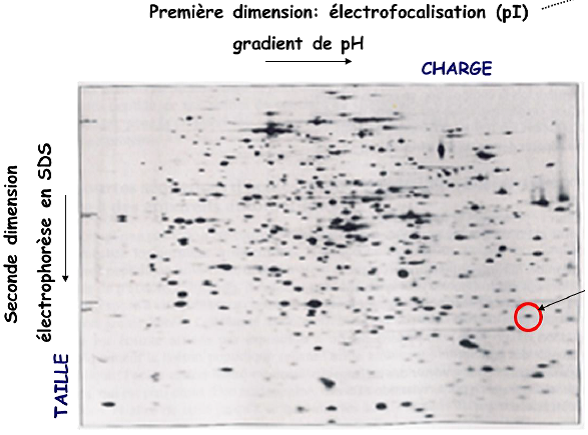
On peut isoler une protéine (cercle rouge) et analyser directement sa composition par spectrométrie de masse (voir section suivante).
5. Analyser la composition chimique de la protéine : composition en acides aminés et séquence
La méthode la plus utilisée pour analyser la composition chimique d’une protéine est aujourd’hui la spectrométrie de masse.
Cette méthode permet de déterminer avec une très grande précision la masse d’une molécule et cela à partir de quantités extrêmement faibles de l’ordre de 10-12 mole (picomole) à 10-15 mole (fentomole).
Dans le cas des protéines, la spectrométrie de masse permet :
- de déterminer la composition en acides aminés des protéines
- de déterminer la séquence des peptides et des protéines, c’est à dire l’ordre dans lequel sont enchaînés les acides aminés.
- de caractériser des mutations y compris des mutations ponctuelles
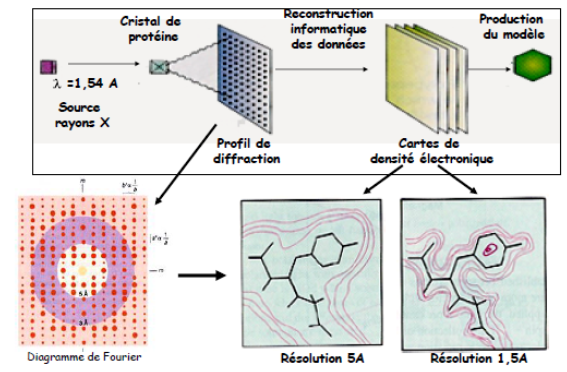
6. Découvrir la structure spatiale de la protéine : diffraction des rayons X
Détermination de la structure spatiale d’une protéine purifiée par formation d’un cristal de protéines qui est soumis aux rayons X.
Le profil de diffraction est analysé pour déterminer la structure tridimensionnelle.
7. Corréler la structure à la fonction de la protéine
Arrivé à ce stade, nous savons :
- Que la plupart des fonctions biologiques sont réalisées par des protéines
- Qu’il est possible d’isoler la/les protéine(s) responsable(s) d’une fonction
- Que cette protéine est un enchaînement (polypeptide) d’unités de base (acides aminés)
- Que les acides aminés se succèdent selon une séquence spécifique
- Que cette séquence spécifique constitue la structure primaire de la protéine
- Que la protéine adopte une structure spatiale, accessible par diffraction X
