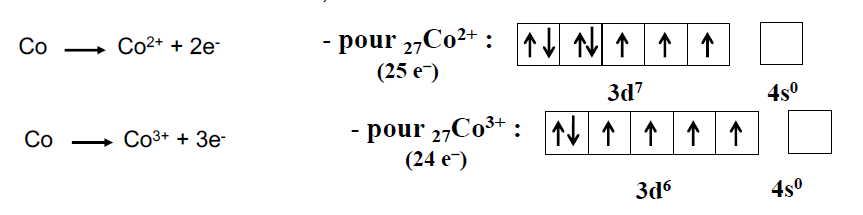Atomistique
Ce que vous savez du lycée
| Du collège | Déjà au collège, vous avez été familiarisés avec des notions de l’échelle microscopique : molécules, atomes et ions, constituants de l’atome (noyau et électrons) et du noyau (neutrons et protons), formule chimique d’une molécule, formules O2, H2, N2, H2O, CO2. |
| De la seconde : | En résumé, vous avez été familiarisés avec les notions suivantes : tableau périodique, analyse de configuration électronique, électrons de valence, stabilité des gaz nobles, ions monoatomiques, modèle de la liaison covalente, lecture de schémas de Lewis de molécules, solution, soluté, solvant, concentration maximale d’un soluté (solubilité). En détails : Dans la partie « Modélisation de la matière à l’échelle microscopique », ont été définies les notions suivantes : espèces moléculaires, espèces ioniques, électroneutralité de la matière au niveau macroscopique, entités chimiques (molécules, atomes, ions). Ainsi, vous savez : – définir une espèce chimique comme une collection d’un nombre très élevé d’entités identiques – exploiter l’électroneutralité de la matière pour associer des espèces ioniques et citer des formules de composés ioniques – utiliser le terme adapté parmi molécule, atome, anion et cation pour qualifier une entité chimique à partir d’une formule chimique donnée. Vous avez également défini le noyau de l’atome, le siège de sa masse et de son identité, avec les notions de numéro atomique et de nombre de masse, ainsi que l’écriture conventionnelle : ZAX ou AX. Les notions d’élément chimique, de masse et charge électrique d’un électron, d’un proton et d’un neutron, de charge électrique élémentaire et de neutralité de l’atome, ont été définies et vous permettent de : – citer l’ordre de grandeur de la valeur de la taille d’un atome. – comparer la taille et la masse d’un atome et de son noyau. – d’établir l’écriture conventionnelle d’un noyau à partir de sa composition et inversement. Vous avez appris que le cortège électronique de l’atome définit ses propriétés chimiques, au travers de sa configuration électronique (1s, 2s, 2p, 3s, 3p) à l’état fondamental et sa position dans le tableau périodique (blocs s et p). Avec les notions d’électrons de valence et de familles chimiques, vous savez ainsi : – déterminer la position de l’élément dans le tableau périodique à partir de la donnée de la configuration électronique de l’atome à l’état fondamental. – déterminer les électrons de valence d’un atome ( – associer la notion de famille chimique à l’existence de propriétés communes et identifier la famille des gaz nobles. Enfin, vous avez appris à compter les entités dans un échantillon de matière et ainsi définir le nombre d’entités dans un échantillon, la mole et la quantité de matière dans un échantillon. Vous savez donc : – déterminer la masse d’une entité à partir de sa formule brute et de la masse des atomes qui la composent. – déterminer le nombre d’entités et la quantité de matière (en mol) d’une espèce dans une masse d’échantillon. Capacités mathématiques demandées : – effectuer le quotient de deux grandeurs pour les comparer. – utiliser les opérations sur les puissances de 10. – exprimer les valeurs des grandeurs en écriture scientifique. |
| De la première : | / |
| De la terminale : | / |
1. Introduction : qu’est-ce que l’atome ?
1.1. Les modes de représentation de l’atome suite aux grandes expériences qui débutent au 19ème siècle
| 1897 : découverte de l’électron par Thomson m = 9.1 x 10-31 Kg |  |
| 1904 : modèle Saturnien de Nagaoka |  |
| 1911 : modèle planétaire de Rutheford Découverte du noyau L’atome est constitué de vide ! |  |
| 1913 : modèle orbitalaire de Bohr | 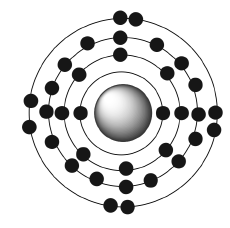 |
| 1926 : modèle quantique de Schrödinger | 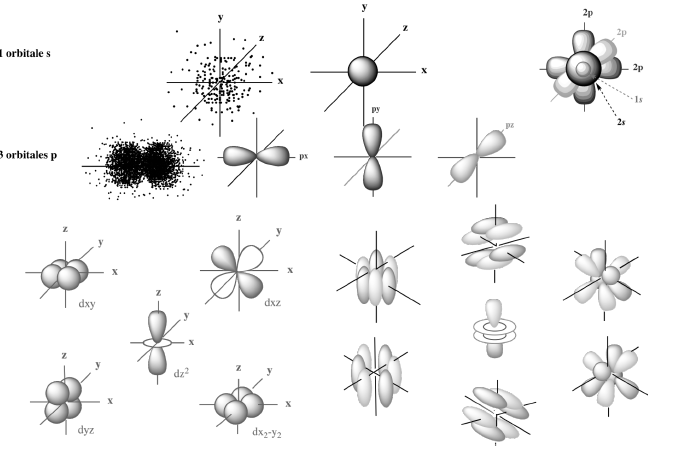 |
1.2. Constitution générale
Dans un atome :
- Les électrons gravitent autour du noyau : 10-10 m = 0.1 nm = 1 Å
- Le noyau est constitué de nucléons neutres (neutrons) et chargés (protons) : 10-14 m
- Les protons et neutrons sont constitués eux-mêmes de quarks up (u) et down (d) : 10-17 m
- Les quarks (2 up et 1 down) sont constitués eux-mêmes de cordes ? ≈ 10-37 m (théorie encore qu’il reste à démontrer)
2. Atome ou élément
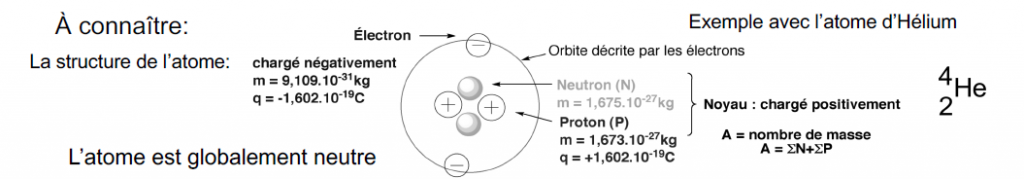
Les espèces atomiques, encore appelées éléments ou nuléides, sont symbolisées de la façon suivante :
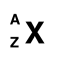
L’élément est défini par :
- A = nombre de masse = nombre de nucléons (protons P + neutrons N)
- Z = numéro atomique = nombre de protons
La masse de l’atome sera fonction du nombre de masse, car la masse de l’électron est négligeable.
Exemple : le nucléide ou l’élément « cuivre »

- Z = nombre de protons = 29
- A = nombre de masse (P + N) = 63
- Nombre de neutrons = 63 -29 = 34
- Nombre d’électrons = 29
=> Les éléments sont classés dans le tableau périodique par numéro atomique croissant :

2.1. Masse réelle des atomes ou éléments : la masse atomique réelle en kg ou en u.m.a
La masse de l’atome est pratiquement égale à celle du noyau, pour deux raisons :
- Les nucléons, neutron et proton, ont une masse quasi-identique (1,67.10-27 kg), l’électron est 1 836 fois plus léger (9,109.10-31 kg)
- Les nucléons sont (atomes d’hydrogène excepté) plus nombreux que les électrons : par exemple, l’atome de carbone a 6 électrons pour 12 nucléons (protons + neutrons).
On obtient par conséquent une mesure assez précise de la masse de l’atome en multipliant son nombre de nucléons (appelé nombre de masse et noté A) par la masse d’un nucléon, environ 1,67.10-27 kg.
La masse d’un atome peut s’exprimer en kg.
Exemple autour de l’atome de carbone :
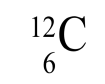
- le nombre de masse = 12
- MP ≈ MN ≈ 1,67.10-27 kg
- Masse atomique de l’atome de carbone ≈ 12 x 1,67.10-27 kg = 2.10-26 kg
La masse d’un atome peut s’exprimer en Unité de Masse Atomique, noté u.m.a ou u :
- L’atome de carbone sert de référence et permet de définir l’u.m.a comme étant égale à 1/12 de la masse d’un atome de carbone : 1 u.m.a ≈ 1,67.10-27 kg ≈ MP ≈ MN
- Ainsi l’atome de carbone 12 a une masse 12u !
| En réalité : – La masse du noyau est inférieure à la somme des masses de chacun de ses nucléons ! – La masse de l’atome de carbone = 1,99625.10-26 kg, inférieure à la somme des masses des nucléons = 2.10-26 kg => 1 u.m.a = 1,66.10-27 kg et non pas 1,67.10-27 kg ! Ce « défaut de masse » se retrouve sous forme « d’énergie » grâce au principe d’équivalence masse-énergie exprimé par Albert Einstein : E = mc2 Certaines transformations de noyaux libèrent de l’énergie de liaison : c’est l’origine de l’énergie nucléaire. Ces transformations sont appelées réactions nucléaires. Elles sont de deux types (fusion nucléaire et fission nucléaire) : – Deux éléments légers (hydrogène, hélium…) produisent un dégagement d’énergie en fusionnant. Cette fusion est à l’origine de l’énergie dégagée par le Soleil. – Les éléments lourds (uranium, plutonium…) ne peuvent dégager de l’énergie que par la fission nucléaire. C’est la réaction de fission qui est mise en œuvre dans les centrales nucléaires. |
Que ce soit en kg ou en u.m.a, cela reste peu pratique à utiliser et il a fallu développer une unité de mesure plus adaptée aux quantités importantes de matière.
2.2. Quantité de matière
Le chimiste travaille en général avec des quantités de matière (atomes, molécules…) importantes, pour lesquelles le nombre d’atomes, de molécules… est gigantesque et nécessite l’utilisation d’une unité de mesure : la mole.
La mole (symbole mol) est une unité de base du système internationale, apparue en 1971, et qui correspond à la quantité de matière (atome, molécule, particules…) d’un système qui contient autant d’entités élémentaires qu’il y a d’atomes de carbone dans 12 g de carbone (1 mole d’atome pèse exactement 12 g/mol).
Sachant qu’un atome de carbone pèse exactement 1,99625.10-26 kg, on en déduit le nombre d’atome de carbone dans 12 g d’atome de carbone 12 :

Ce nombre porte le nom de constante d’Avogadro, en hommage à Lorenzo Romano Amedeo Carlo Avogadro, physicien et chimiste (1776-1856).
La mole est une unité de comptage au même titre que la dizaine, la centaine… mais cette unité de comptage est immense (602 214 milliards de milliards d’unité). De la même manière qu’il y a autant d’éléments dans une douzaine de plumes que dans une douzaine d’œufs, il y a le même nombre de carbone que dans une mole de plomb (c’est-à-dire 602 214 milliards de milliards d’atomes), mais la masse de ces moles sera différente car la masse des atomes sera différente !
2.3. Masse molaire d’un élément : c’est la masse d’une mole de cet élément !
Exemple :
Masse atomique réelle d’un atome du nucléide 14N ≈ 14 uma soit 14 x 1,67.10-27 kg = 2.33.10-26 kg (ou 2.3210-26 kg si l’on considère 1 u.m.a = 1,67.10-27 kg…)
Masse molaire de 14N correspond à la masse d’une mole d’atomes 14N, c’est-à-dire de 6,02.1023 atomes de 14N et donc 2,33.10-26 x 6,02.1023 ≈ 14 g.mol-1
=> La masse d’une mole (masse molaire) d’un élément X s’exprime en gramme / mol.
2.4. Masse molaire d’une molécule aussi…
Elle correspond à la somme des masses molaires des atomes qui constituent la molécule.
Exemple : M(H2O) = (1 x 2) + 16 = 18 g.mol-1
3. Isotope
Pour un élément (atome) donné, le nombre de protons Z (ou numéro atomique) restera invariable.
En revanche, il existe des variations dans le nombre de neutrons et le nombre d’électrons définissant le passage de l’atome à respectivement l’isotope ou l’ion. Ces caractéristiques permettent de définir l’isotope et l’ion pour un élément donné.
Des nucléides ayant le même nombre de proton Z et différents par leur nombre de masse (donc par leur nombre de neutrons) correspondent au même élément et sont qualifiés d’isotopes de l’élément en question.
Exemple : l’élément Hydrogène (H)
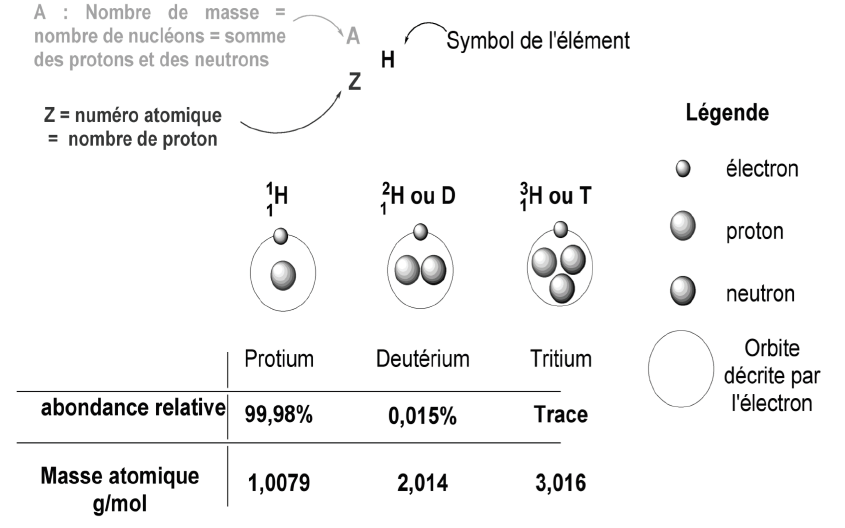
C’est grâce à cette différence d’abondance relative des isotopes d’hydrogène que les instruments de la sonde Rosetta ont permis de déterminer que l’eau de la comète qu’elle scrute est différente des eaux terrestres.
3.1. Isotope et radioactivité
Isotope ne signifie pas systématiquement élément radioactif ! Par exemple, les isotopes 1H et 2H de l’élément Hydrogène sont stables. Seul l’atome de tritium est radioactif : il se désintègre en émettant un rayonnement.
La radioactivité a été découverte par Marie Curie, première femme à recevoir le Prix Nobel de chimie en 1903, pour la découverte du radium et du polonium, à l’origine de sa mort.
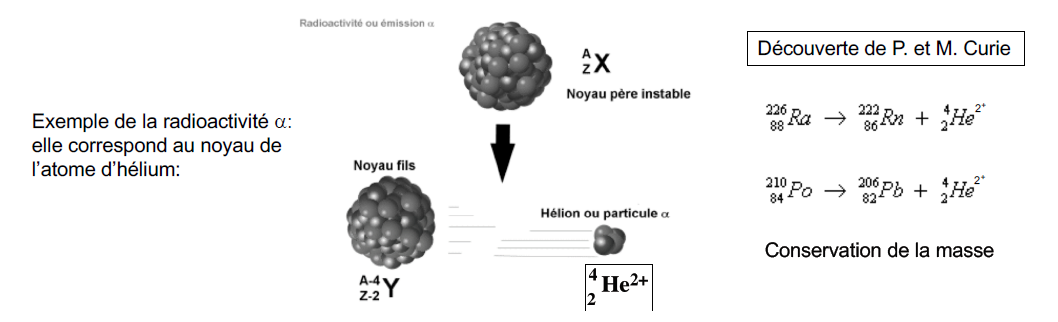
La radioactivité naturelle est un processus spontané qui conduit à la fission du noyau d’un atome instable (père). Cette fission engendre un nouvel atome plus stable (fils) accompagné par l’émission de particules énergétiques α ou β- ou β+ ou d’un rayonnement γ (voir fiche de cours sur la radioactivité dans le module de physique).
Exemple de la radioactivité α : elle correspond au noyau de l’atome d’hélium.
3.2. Masse moyenne des atomes ou éléments
Masse de cet élément en u.m.a pondérée par l’abondance de ses isotopes ou l’abondance isotopique.
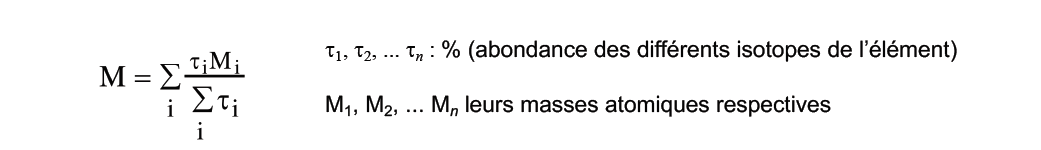
Exemple : l’élément chlore naturel contient 75 % de l’isotope 35Cl et 25 % de l’isotope 37Cl.
La masse atomique moyenne est :
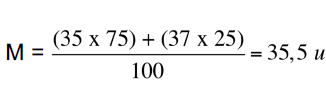
4. Qu’en est-il de l’électron ?
Négligé pour le moment dans la description de l’atome, c’est un acteur essentiel de la structure moléculaire et de la réactivité. En effet, en chimie, la réactivité est décrite à travers son comportement.
L’ion :
- est une entité chargée.
- se forme lors d’une réaction chimique, lorsque l’atome perd ou gagne un ou plusieurs électrons.
- portera alors respectivement une charge positive ou négative
- sera qualifié de cation (+) ou d’anion (-).
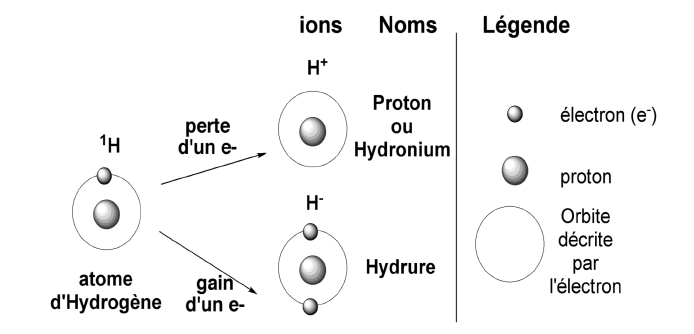
Dans le cas de l’atome d’hydrogène, le cation porte le nom de proton (puisqu’il n’est constitué que d’un seul proton et ne comporte pas de neutron), encore appelé hydronium, et l’anion porte le nom d’hydrure.
Dans le modèle planétaire de Rutherford de 1911, l’électron peut occuper des orbites de rayon quelconque laissant supposer que son spectre d’émission serait un continuum présentant l’ensemble des longueurs d’onde accessibles, tel un arc-en-ciel. Or les travaux effectués sur l’hydrogène avaient mis en évidence un spectre de raies discontinues, modélisé par Bohr en 1913 sous le nom, modèle orbitalaire.
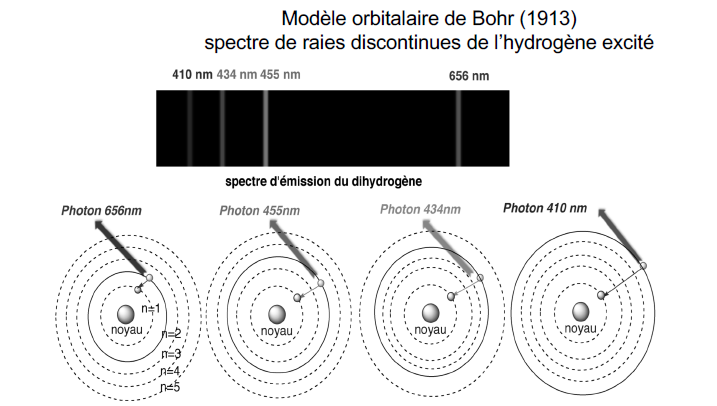
Dans ce dernier, les électrons ne peuvent circuler que sur des orbites privilégiées stationnaires n de rayon e Bohr r = n2 x 0.53 Å pour lesquelles ils ne rayonnent pas d’énergie.
Que se passe-t-il d’un point de vue énergétique ?
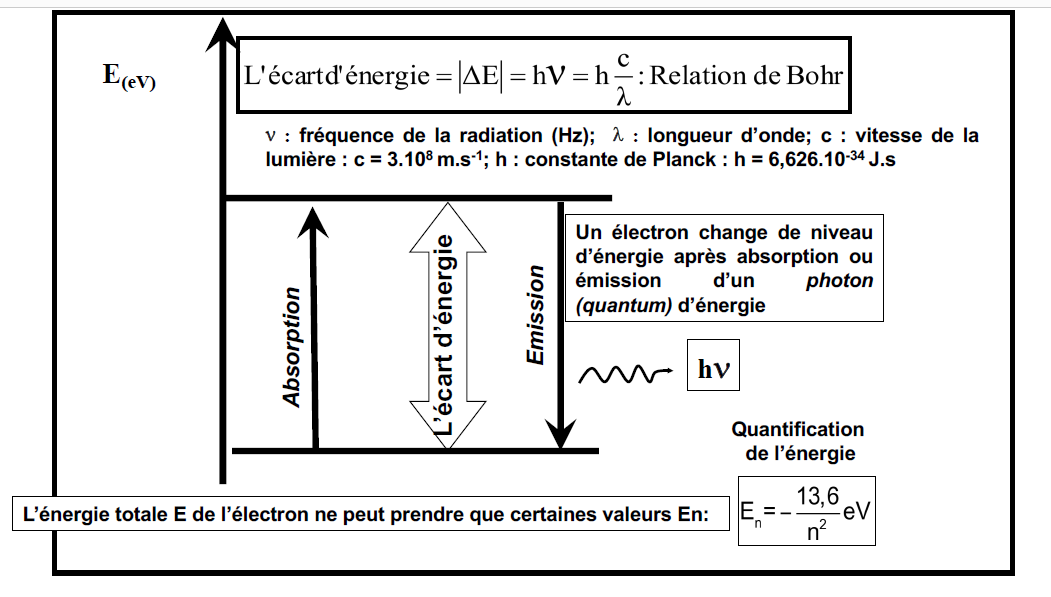
- Les électrons ne peuvent circuler que sur des orbites privilégiées stationnaires pour lesquelles ils ne rayonnent pas d’énergie.
- Ces orbites sont qualifiées de niveaux (ou de couches) n.
- L’énergie de chaque niveau croit en fonction de la distance par rapport au noyau.
- Le passage d’un niveau à un autre s’accompagne obligatoirement de l’émission ou l’absorption d’une radiation électromagnétique : lumière visible, ultra-violet, rayonnement X.
Remarque : Ces modèles planétaire ou orbitalaire de l’atome sont faux, car ils supposent qu’il est possible de déterminer la trajectoire de l’électron (vitesse et position simultanément). Or Heisenberg a démontré que c’était impossible.
Erwin Schrödinger développe alors une équation différentielle, portant désormais son nom, qui permet de décrire précisément l’évolution quantique d’une particule, en déterminant sa probabilité de présence dans un espace.
=> Les solutions de cette équation au carré décrivent des domaines de l’espace où la probabilité de trouver un électron est supérieure à 95%. Ces domaines portent le nom d’orbitale atomique.
Les orbitales atomiques portent un nom :
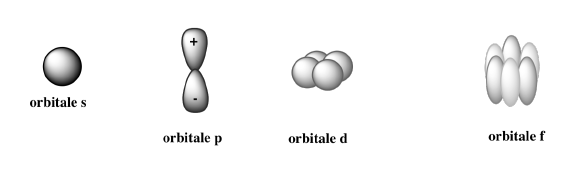
Sharp, Principal, Diffuse, Fundamental…
L’état quantique ou « l’identité » d’un électron sera défini par 4 nombres quantiques (n, l, m, s) permettant de délimiter les domaines de l’espace ou orbitales atomiques où la probabilité de présence de ce dernier sera supérieur à 95 % :
| n : nombre quantique principal | – Numéro de la couche quantique à laquelle appartient l’électron – – Définissant le niveau d’énergie auquel l’électron appartient, pour un atome dans son état fondamental Dans le cas de l’hélium ci-dessous, la couche n=1 (ou K) contient deux électrons. Elle est ainsi saturée. A ce stade, rien ne distingue ces 2 électrons. 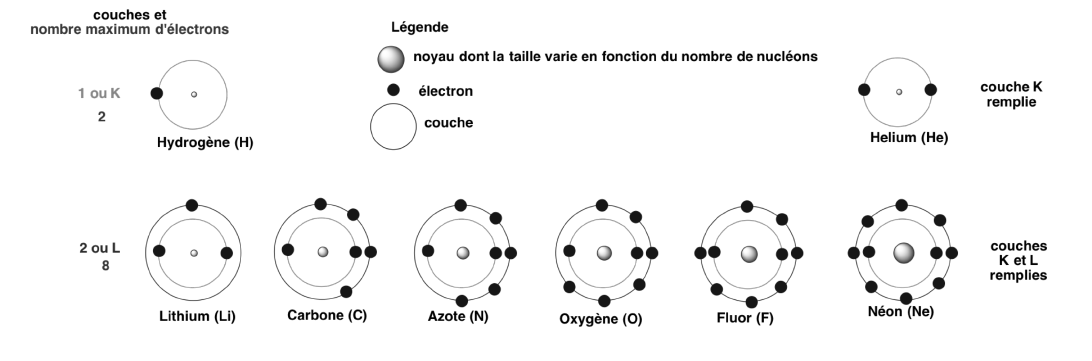 Remarque : si |
| l : nombre quantique secondaire | Dans le niveau n ou couche, l’électron occupe des sous-niveaux d’énergie ou des sous-couches qui définissent les orbitales à travers I. l est fonction de n et prend toutes les valeurs de 0 à n-1. Dans la couche ou orbite, il décrit les formes des fameuses orbitales, c’est-à-dire les domaines de l’espaces où la probabilité de trouver un électron est supérieur à 95% : – l = 0 et le domaine de l’espace où la probabilité de trouver un électron correspond à l’orbitale atomique s (sharp) – l = 1 définit l’orbitale p (principal) – l = 2 définit l’orbitale d (diffuse) – l = 3 définit l’orbitale f (fundamental) – puis l = 4, 5, 6 (pour les états excités) définissent les orbitale g, h ,i (suite alphabétique de f) Représentation pour s, p, d, et f : 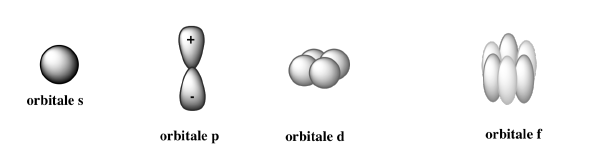 |
| m : nombre quantique magnétique | Il peut prendre toutes les valeurs comprises entre –l et +l. Il détermine les orientations possibles de l’orbitale atomique dans l’espace. Exemple : – l = 0 (pour n = 1) => m = 0 => 1 seule orientation => 1 orbitale s 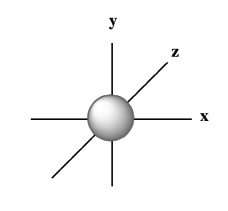 – l = 1 => m = -1, 0, 1 => 3 orientations suivant 3 axes x, y et z => 3 orbitales p de même énergie, les orbitales sont dites dégénérées (même énergie) : 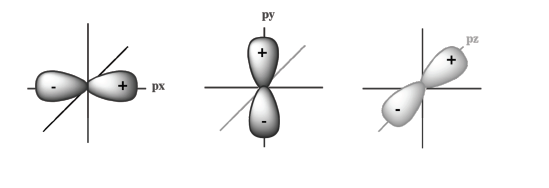 – l = 2 => m = -2, -1, 0, 1, 2 => 5 orbitales atomiques possibles => 5 orbitales d de même énergie : 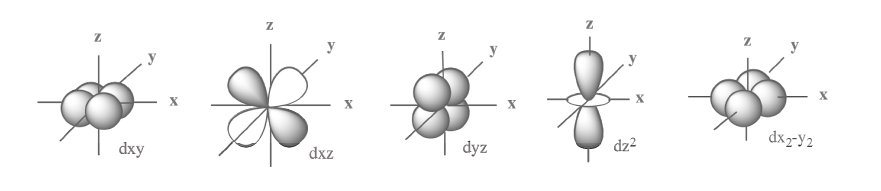 – l = 3 => m = -3, -2, -1, 0, 1, 2, 3 => 7 orbitales atomiques possibles => 7 orbitales f de même énergie : 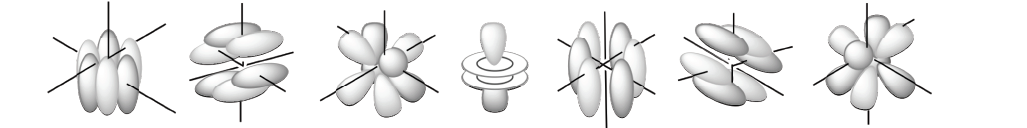 Pour faciliter l’écriture des orbitales, on utilise des cases quantiques : 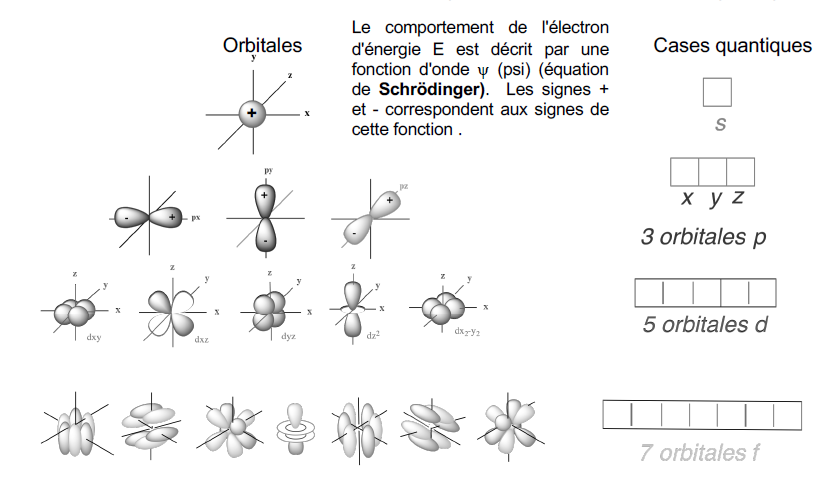 Important : Chaque orbitale ne peut contenir que 2 électrons. Donc 2 électrons maximum dans l’orbitale s, 3 x 2 = 6 électrons dans les 3 orbitales p au maximum… Mais comment distingue-t-on ces électrons quand ils sont appariés ??? => Grâce au dernier nombre quantique s… |
| s : nombre quantique de spin | Dû à la rotation de l’électron sur lui-même. Deux orientations sont possibles suivant le sens de rotation de l’électron sur lui-même : – – Exemple : Ainsi, si l’on récapitule dans le cas de l’atome d’Hélium qui possède la structure 42He, 2 protons donc 2 électrons qui occuperont la couche 1 ou K, saturée avec ces deux électrons. n = 1 Alors l prend toutes les valeurs de 0 à n-1, donc ici l = 0. Or si l = 0, m = 0 et les 2 électrons seront localisés dans une seule et même orbitale de type s. => Attention à ne pas confondre l’orbitale s avec le nombre quantique de spin s !!! Un principe : Wolfgang Pauli énonça en 1925 un principe selon lequel deux électrons d’un même atome ne peuvent pas se trouver simultanément dans le même état quantique, ce qui signifie qu’ils ne peuvent pas avoir leur 4 nombres quantiques identiques et vont donc au minimum se distinguer par leur nombre quantique de spin s qui seront de signes opposés ! |
En résumé, la carte d’identité ou formalisme d’écriture :
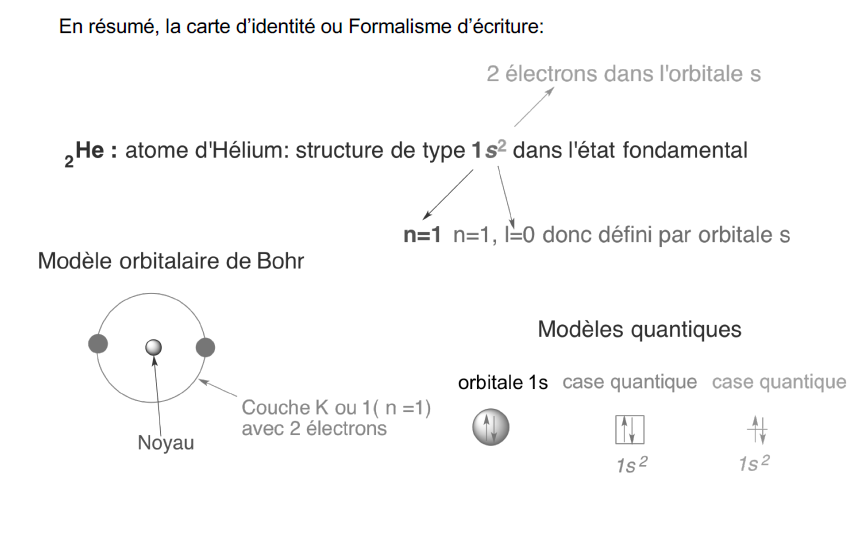
4.1. Qu’en est-il pour les atomes plus complexes ? Comment se répartissent les électrons des orbitales pour les éléments au-delà de n = 2 ? Quels sont les principes et les règles ? Comment procède-t-on ?
Modèle orbitalaire de Bohr appliqué à tous les éléments
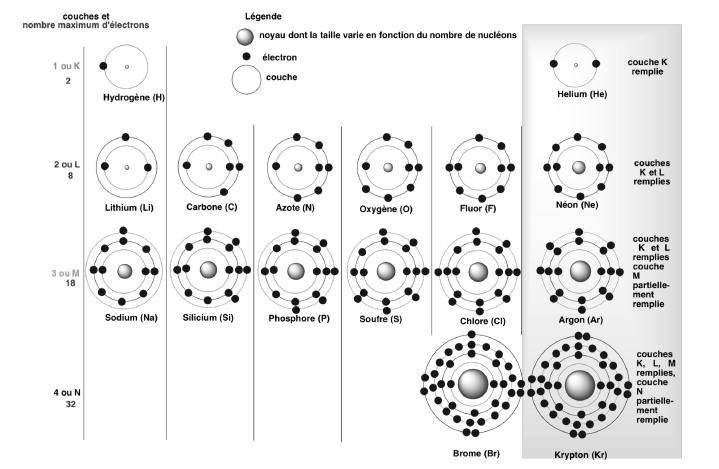
- Principe d’exclusion de Pauli : deux électrons d’un même atome ne peuvent pas avoir leurs quatre nombre quantiques identiques.

- Principe de stabilité : à l’état fondamental, un atome se trouve dans son état énergétique le plus stable correspondant à l’énergie la plus basse.
=> Hydrogène et hydrogénoïdes : noyau associé à un électron
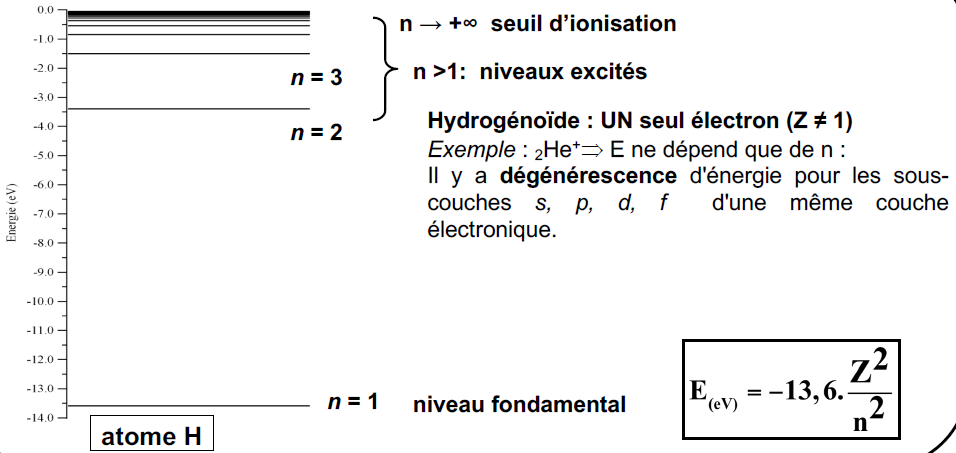
=> Atomes poly-électrononiques
E dépend de n et de l : il y a levée de la dégénérescence des sous-couches s, p, d, f d’une même couche électronique. Les électrons d’un même niveau occupent des orbitales dont l’énergie est différente et dont la valeur dépend des nombres quantiques n+l.
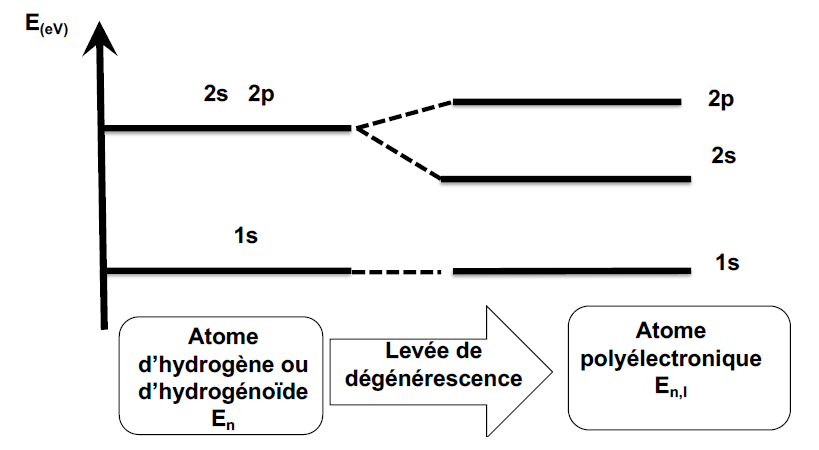
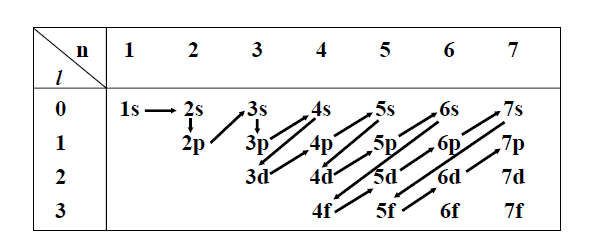
- La règle de Klechkowski : (n+l) minimal

L’ordre de remplissage des orbitales n’est pas linéaire et la règle de Klechkowski (n+l) définit l’ordre de remplissage.
Cas des sous-couches 4s et 3d
4s : n =4 ; l = 0 => n+l = 4
3d : n= 3 ; l = 2 => n+l = 5
(n+l)4s < (n+l)3d => E4s < E3d
Les électrons occupant d’abord le niveau « 4s » avant le niveau « 3d »n, de même entre les niveaux « 5s » et « 4d ».
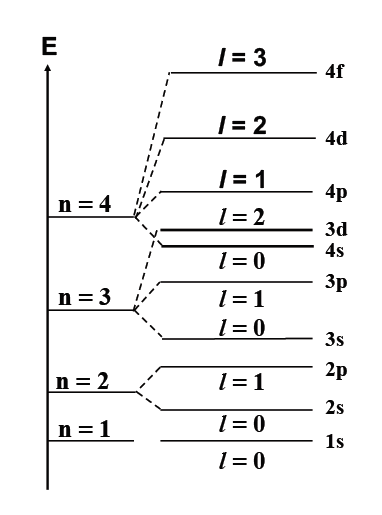
Parmi les sous-couches encore vides, la premières à se remplir est celle pour laquelle (n+l) est la plus faible.
Exemple : les sous-couches de la couche L (n = 2) se remplissent dans l’ordre suivant : 2s (2 + 0 = 2) puis 2p (2 + 1 = 3).
Si deux sous-couches vides sont caractérisées par la même valeur de la somme (n+l), celle de plus faible nombre quantique principal n se remplit la première.
Exemple : les sous-couches 2p (2 + 1 = 3) et 3s (3 + 0 = 3) se remplissent dans l’ordre suivant : 2p puis 3s.
| Niveaux d’énergie et couches électroniques | Sous-couches et nombre maximal d’électrons par sous-couche | Nombre d’électrons total = 2n2 |
| n = 1 : couche K | s2 | 2 |
| n = 2 : couche L | s2 p6 | 8 |
| n = 3 : couche M | s2 p6 d10 | 18 |
| n = 4 : couche N | s2 p6 d10 f14 | 32 |
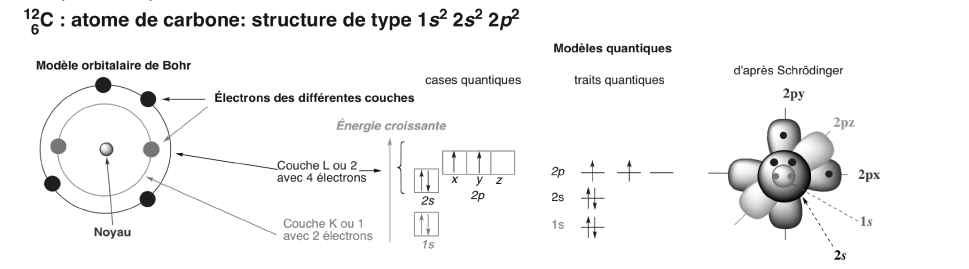
Exemple 1
L’atome de carbone ![]() porte 6 protons donc 6 électrons qui se répartiront dans la couche 1 ou K (saturée avec deux électrons) et la couche 2 ou L (saturée avec 8 électrons).
porte 6 protons donc 6 électrons qui se répartiront dans la couche 1 ou K (saturée avec deux électrons) et la couche 2 ou L (saturée avec 8 électrons).
=> La couche 2 sera donc partiellement occupée par 4 électrons dans le cas de l’atome de carbone !

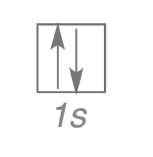
Pour n = 1, l = 0 et m = 0, et deux électrons au maximum de spin s opposés occupent cette orbitale s notée 1s2.
Pour n = 2, l = 0 et 1 :
- Pour l = 0, nous aurons 1 orbitale s notée 2s qui contiendra 2 électrons : 2s2
- Pour l = 1, m = -1, 0, +1 définissant les 3 orbitales p : px, py, pz, de même énergie et notées 2px, 2py et 2pz, pouvant contenir au maximum 3×2 électrons = 6 électrons. Il ne reste cependant que 2 électrons à placer : 2p2.
Exemple 2
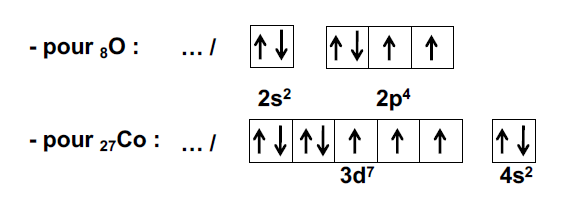
8O (8 électrons à placer) : 1s2 / 2s2, 2p4 => électrons de cœur / électrons de valence
Ecriture simplifiée : 8O : [2He], 2s2, 2p4, car 1s2 correspond à la structure électronique du gaz rare le plus proche.
Il est essentiel d’identifier et quantifier les électrons de valence qui seront les seuls à intervenir pour décrire la réactivité chimique.
Le nombre d’électrons de valence pour les éléments dont la configuration électronique se termine par nsx ou (nsx, npy) est donné par le nombre total d’électrons sur le niveau n le plus élevé :
- nsx : x électrons de valence
- (nsx, npy) : (x = y) électrons de valence
Exemple 3
27Co (27 électrons à placer) : 1s2, 2s2, 2p6, 3s2, 3p6 / 4s2, 3d7, en tenant compte de la règle du (n+l) minimal.
Mais attention ! On écrit 3d7, 4s2, au lieu de 4s2, 3d7 car les électrons 4s sont plus facilement éjectés que les électrons d (assez général pour la 4ème période), lors de la formation des cations.
Ecriture simplifiée : 27Co : [18Ar], 3d7, 4s2
Le nombre d’électrons de valence pour les éléments dont la configuration électronique se termine par [nsx, (n-1)df] est donné par le nombre total d’électrons sur le niveau ns le plus élevé et sur celui de (n-1)d :
[nsx, (n-1)df] : (x + y) électrons de valence, soit ici pour Co, 9 électrons de valence.
4.2. Comment écrire la structure électronique ou configuration électronique à l’état fondamental ? Les affinements de la règle :
4.2.1. L’occupation maximale des orbitales est une source de stabilisation.
Le chrome : 24Cr : 1s2, 2s2, 2p6, 3s2, 3p6 / 3d5, 4s1, et non pas 3d4, 4s2
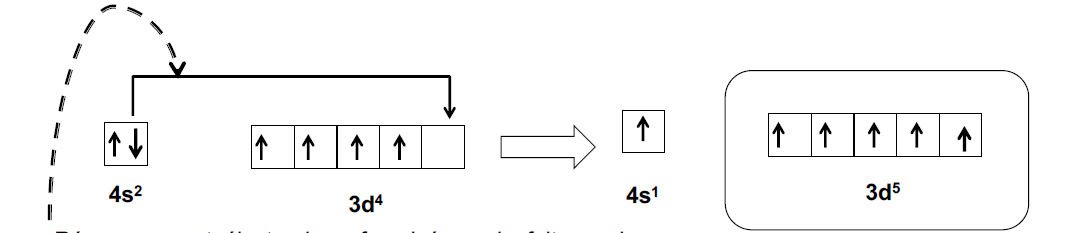
=> Système stabilisé (Hund)
Réarrangement électronique favorisé par le fait que les niveaux 4s et 3d sont très proches les uns des autres et pour mémoire, les orbitales sont les domaines de l’espace où la probabilité de trouver un électron est supérieure à 95% et l’occupation maximale de ces espaces est favorable, bien que 4s soit relativement plus stable que 3d (proximité !).
Stabilisation valable également pour le molybdène.
4.2.2. L’occupation maximale des orbitales d est une source de stabilisation.
Le cuivre : 29Cu : 1s2, 2s2, 2p6, 3s2, 3p6 / 3d10, 4s1, et non pas 3d9, 4s2
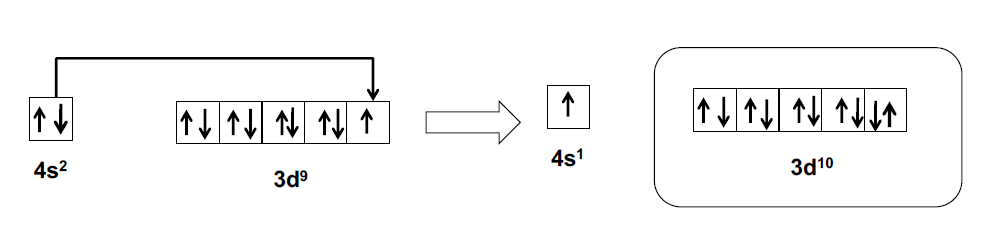
=> Système stabilisé (Hund)
Stabilisation valable également pour l’argent.
4.2.3. Règle de Hund (règle du spin maximal)
Lorsque des orbitales atomiques ont même énergie (dégénérées, exemple avec npx, npy et npz), les électrons se répartissent avec un nombre maximum de spins parallèles.
Utilisation des cases quantiques symbolisant chacune une orbitale atomique.
Pour écrire la structure électronique d’une espèce cationique (perte d’électron !!) :
- Cas général : on enlève d’abord les électrons les plus externes (ceux qui correspondent à n le plus grand).
- Dans le cas des métaux de transition, on enlève donc d’abord les électrons « s ». Ainsi :

Exemple 4
La structure électronique du cuivre peut s’écrire :
- 29Cu : 1s2, 2s2, 2p6, 3s2, 3p6 / 3d10, 4s1
- 29Cu : [18Ar], 3d10, 4s1
Celle du 29Cu+ : 1s2, 2s2, 2p6, 3s2, 3p6 / 3d10, 4s0
Celle du 29Cu2+ : 1s2, 2s2, 2p6, 3s2, 3p6 / 3d9, 4s0
5. Le tableau de classification périodique
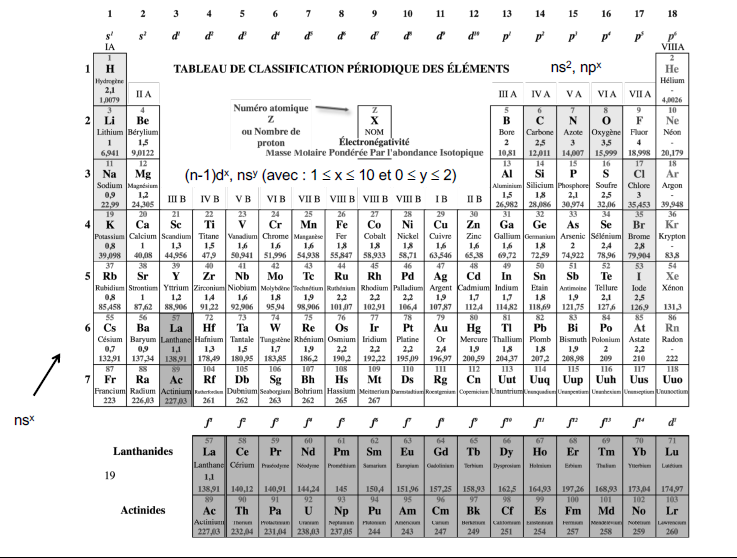
5.1. Les familles ou colonnes
Colonne 1 : les alcalins => la structure électronique externe est ns1.
Colonne 2 : les alcalino-terreux => la structure électronique externe est ns2.
Colonnes 3 à 12 : les métaux de transition
Colonne 17 : les halogènes => la structure électronique externe est ns2, np5.
Colonne 18 : les gaz rares => la structure électronique externe est ns2, np6 (sauf pour l’hélium => ns2). La configuration du gaz rare correspond à la saturation de la couche électronique.
Comment identifier la famille d’un élément à partir de sa structure électronique ?
=> numéro d’une colonne (à partir du nombre d’électrons sur nmax) :
- Structure électronique externe est ns1 = colonne 1
- Structure électronique externe est ns2 = colonne 2
- Structure électronique externe est nsx, npy = colonne (10 + x + y)
5.2. Les périodes ou lignes
Les éléments d’une même ligne dans la table périodique constituent une période.
Le numéro de la période correspond au nombre quantique principal n le plus élevé pour un élément donné.
Exemple avec l’atome d’oxygène :
8O : 1s2 / 2s2, 2p4 => n = 2, l’oxygène est donc sur la deuxième ligne.
- Nombre de couches électroniques = 2 : l’oxygène appartient à la deuxième période (deuxième ligne horizontale)
- Nombre d’électron sur la couche de valence (n = 2) 2 + 4 = 6 électrons de valence. L’oxygène appartient donc à la colonne 16 (10 + x + y).
Les éléments appartenant à une même période ont le même nombre de couches électroniques.
6. Ions : cations et anions
L’ion est une entité chargée.
Il se forme lors d’une réaction chimique, lorsque l’atome perd ou gagne un ou plusieurs électrons.
Il portera alors respectivement une charge positive ou négative et sera qualifié de cation (+) ou d’anion (-).
Dans le cas de l’atome d’hydrogène, le cation porte le nom de proton puisqu’il n’est constitué que d’un seul proton et ne comporte pas de neutron, encore appelé hydronium, et l’anion porte le nom d’hydrure.
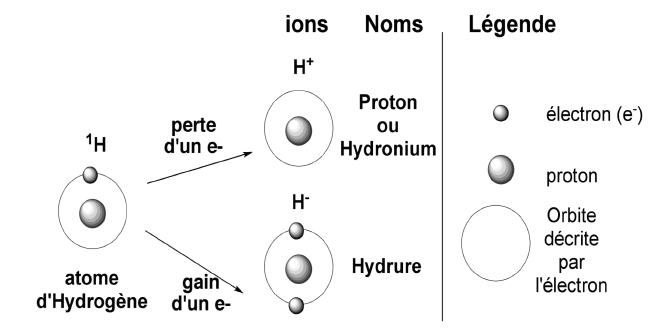
L’énergie nécessaire a été mesurée à l’état gazeux pour un atome isolé. C’est l’énergie d’ionisation.
6.1. Les atomes perdent un ou plusieurs électrons : c’est le phénomène d’ionisation qui génère des cations
L’énergie de première ionisation, EI1, est l’énergie minimale qu’il faut fournir à un atome isolé, A(g) (état gazeux), pour lui arracher un électron selon la réaction :
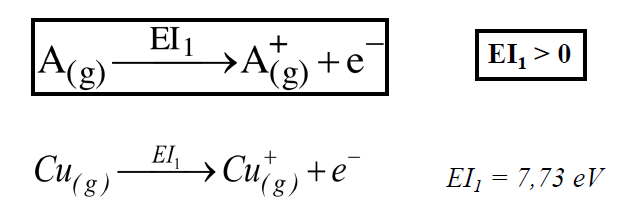
L’énergie de nième ionisation, EIn, correspond à la réaction :

L’énergie d’ionisation est variable d’un élément à l’autre dans le tableau de classification périodique :
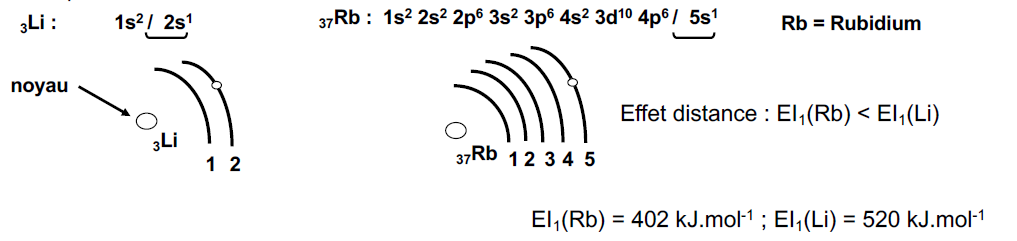
- L’énergie d’ionisation diminue dans une colonne lorsque Z augmente (en allant de haut en bas) car :
- Le nombre de couche électronique augmente.
- La distance noyau – électron périphérique augmente (le rayon atomique augmente) => « effet distance ».
- La force d’attraction noyau – électron périphérique diminue (électron de plus en plus libre).
=> l’énergie d’ionisation diminue.
Exemple :
- Dans une période, l’énergie d’ionisation augmente dans lorsque Z augmente (en allant de gauche à droite) :
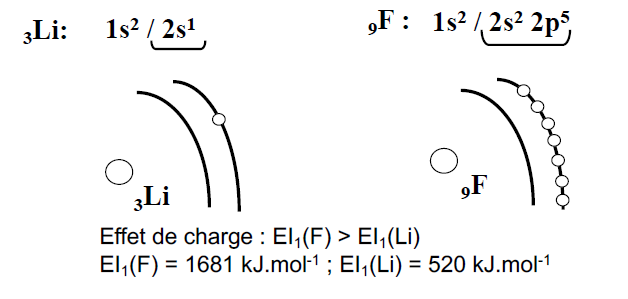
- Le nombre de couches est le même, mais Z augmente (le nombre de charge + dans le noyau augmente) => « effet de charge ».
- La force d’attraction noyau – électron périphérique augmente.
- La distance noyau – électron périphérique diminue (le rayon atomique diminue).
=> l’énergie d’ionisation augmente (mais pas de façon linéaire).
Exemple :
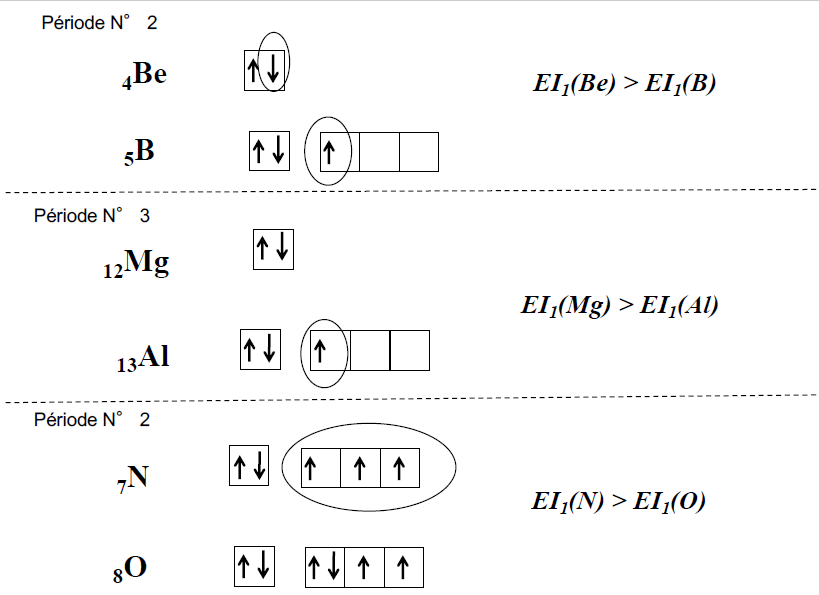
L’énergie d’ionisation d’une période dépend de l’orbitale qui perd l’électron et ne croit pas de façon linéaire :
Pour résumer :

6.2. Les atomes gagnent des électrons : c’est le phénomène d’ionisation qui génère des anions
L’affinité électronique AE est l’opposé « en signe » de l’énergie de fixation électronique Efix d’un électron sur un atome isolé A(g) => AE = – Efix
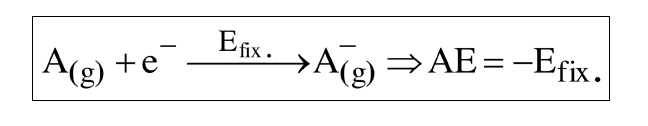
Contrairement à l’énergie d’ionisation, l’affinité électronique peut être positive ou négative.
Si AE > 0 : A–(g) a alors une énergie plus faible que A(g) :l’ion A–(g) est plus stable que A(g)
6.3. Certains atomes ont donc tendance à céder un ou des électrons, d’autres préfèrent gagner un ou des électrons. Dans tous les cas, ces atomes sont faits pour s’associer… et conduire à des édifices moléculaires…
La fonction de l’électronégativité est une grandeur qui mesure l’aptitude du noyau d’un élément (atome) à attirer vers lui les électrons. Des échelles (Mulliken ou Pauling, basée sur les énergies d’ionisation et l’affinité électronique ou les énergies de dissociation des liaisons) attribuent ainsi une valeur pour chaque élément de la classification périodique :
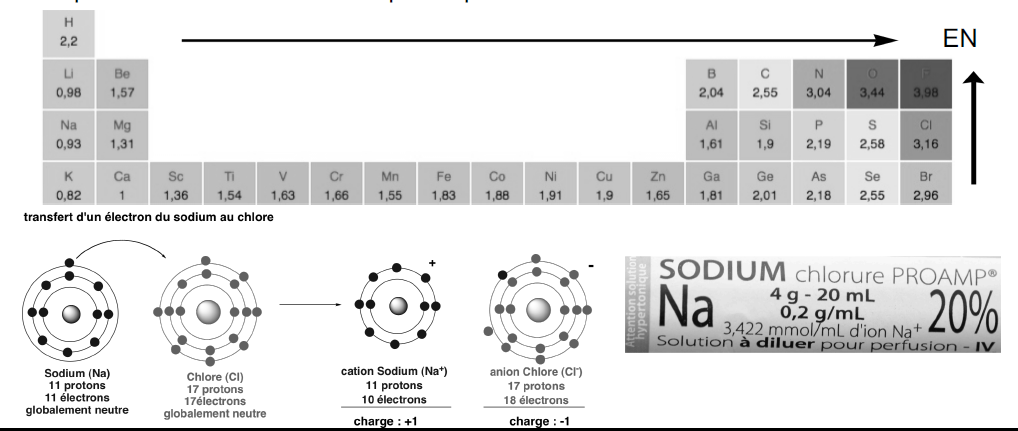
Les éléments de classification périodique vont se combiner afin d’acquérir une structure stable à huit électrons dans la couche externe : c’est la règle de l’octet.
Cette combinaison des atomes conduit à la formation de liaisons chimiques dont la nature est fonction de l’électronégativité des éléments : liaison ionique ou covalente.
- Echelle de Mulliken
L’électronégativité d’un élément dans l’échelle de Mulliken est égale à la moyenne arithmétique de l’énergie de première ionisation, EI1, et de l’affinité électronique, AE.
- Echelle de Pauling
Elle est basée sur les énergies de dissociation des liaisons (Ed) de molécules diatomiques simples : EA-A, EB-B et EA-B : énergies en kJ.mol-1 pour rompre les liaisons A-A, B-B et A-B.
Quelques valeurs des électronégativités dans l’échelle de Pauling
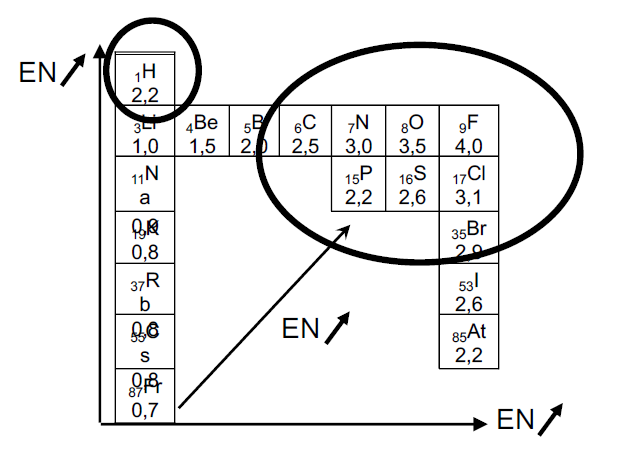
L’électronégativité augmente :
- De gauche à droite dans une période
- De bas en haut dans une colonne.