Structure des protéines : de l’acide aminé à la macromolécule
1. Introduction
Les protéines : premières actrices du monde vivant.
- « protéine » vient de proteion (proteion) = qui occupe le premier
- Il n’existe pratiquement pas de processus biologique non régi par une/des protéine(s).
- Comprendre le fonctionnement d’une protéine, c’est donc comprendre in fine « la logique du vivant »
Les protéines assurent l’ensemble des fonctions du vivant.
| Créer et maintenir une structure | Les protéines du cytosquelette Les protéines des tissus de soutien |
| Reconnaître et se défendre | Les immunoglobulines |
| Transporter | Les transporteurs de petites molécules dont l’oxygène Les transporteurs transmembranaires |
| Transformer | Les enzymes catalysent l’essentiel des réactions chimiques du vivant |
| Bouger – Se déplacer | Les protéines à fonction motrice Les protéines des mouvements intracellulaires |
| Informer – Signaler | Les récepteurs et leurs ligands Les « interrupteurs moléculaires » |
2. Les forces impliquées dans la structure des protéines
Les liaisons covalentes et non covalentes (= liaisons faibles) interviennent dans la structure des protéines.
Dans les molécules biologiques existent des interactions moléculaires non covalentes facilement réversibles. Ces liaisons sont considérablement affectées par la présence de l’eau dans les milieux biologiques.
Les liaisons faibles sont :
- de 4 types
- de faible énergie
- dépendante de la présence d’eau.
| Liaisons | Caractéristiques |
| de Van der Waals | dépendant de la distance inter-atomique |
| Electrostatiques (= ioniques ou salines) | se forment entre molécules chargées |
| Hydrogène | se forment entre molécules polaires (chargées ou non). Dans les protéines, deux types de liaisons hydrogène (LH) :  |
| Hydrophobes | Interaction entre molécules apolaires pour laisser le plus de liaisons hydrogène possibles entre les molécules d’eau (forte affinité de l’eau pour elle-même). Il faut penser à deux gouttes d’huile dans de l’eau. Dans un environnement biologique, les protéines exposent leurs résidus hydrophiles à l’extérieur et les résidus hydrophobes à l’intérieur. Cette règle est pratiquement générale, à l’exception notable des protéines transmembranaires, et constitue l’une des bases principales pour la mise en place de la structure tri dimensionnelle des protéines |
3. Les éléments de bases des protéines : les acides aminés
3.1. Caractéristiques générales
La structure commune de (presque) tous les acides aminés peut s’écrire :
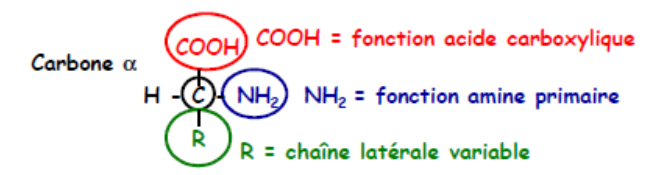
Le carbone α centrale est asymétrique et porte 4 substituants différents :
- Fonction amine : NH2
- Fonction acide carboxylique : COOH
- Hydrogène : H
- Radical (= chaîne latérale) : R
Il existe donc deux stéréoisomères : 2 configurations possibles L et D
Stéréoisomères : les groupements chimiques sont identiques mais placées de manière différente sur la molécule
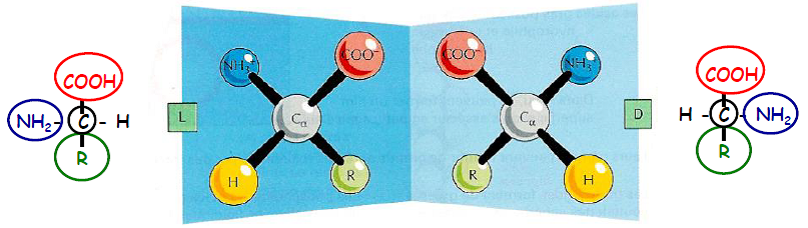
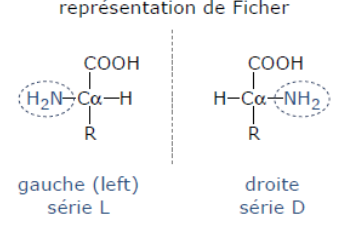
Les acides aminés naturels sont de la série L.
Remarque : La glycine est le seul acide aminé sans carbone α asymétrique.
3.2. Classification des acides aminés
Il existe 20 acides aminés entrant dans la composition des protéines.
On peut répartir les acides aminés selon la nature de leur chaîne latérale en 3 classes qui se subidivisent :
- Acides aminés apolaires
- à chaîne aliphatique : glycine, alanine, valine, leucine , isoleucine, méthionine, proline
- à chaîne aromatique : phénylalanine, tryptophane
- Acides aminés polaires neutres
- à fonction alcool : sérine, thréonine, tyrosine
- à fonction soufrée : cystéine
- à fonction amide : glutamine, asparagine
- Acides aminés polaires ionisables
- à fonction acide : acide glutamique, acide aspartique
- à fonction basique : histidine, lysine, arginine
Il existe des codes à trois ou une lettre extrêmement utilisés pour les séquences protéiques.
Acides aminés apolaires
| Glycine | Gly | G |
| Alanine | Ala | A |
| Valine | Val | V |
| Leucine | Leu | L |
| Isoleucine | Iso | I |
| Méthionine | Mét | M |
| Phénylalanine | Phé | F |
| Tryptophane | Trp | W |
Acides aminés polaires neutres
| Sérine | Sér | S |
| Thréonine | Thr | T |
| Tyrosine | Tyr | Y |
| Cystéine | Cys | C |
| Glutamine | Gln | Q |
| Asparagine | Asn | N |
Acides aminés polaires ionisables
| Acide glutamique | Glu | E |
| Acide aspartique | Asp | D |
| Histidine | His | H |
| Lysine | Lys | K |
| Arginine | Arg | R |
Les 9 acides aminés essentiels ne sont pas synthétisés par l’Homme et sont donc apportés par l’alimentation :
- Valine (Val)
- Leucine (Leu)
- Isoleucine (Iso)
- Méthionine (Met)
- Phénylalanine (Phé)
- Tryptophane (Trp)
- Thréonine (Thr)
- Histidine (His)
- Lysine (Lys)
Moyen mnémotechnique pour apprendre les acides aminés essentiels : Hystérique le très lyrique Tristan fait vachement méditer Iseult (His, Leu, Thr, Lys, Trp, Phe, Val, Met, Ile)
3.3. Propriétés spécifiques des acides aminés apolaires à chaîne aliphatique
| Acides aminés | Représentation de leurs états d’ionisation à pH 7.0 (voir fiche de cours « Etats d’équilibre acido-basique ») | Propriétés spécifiques |
| Glycine | 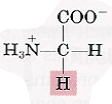 | – Pas de carbone asymétrique – Pas de stéréoisomère |
| Alanine | 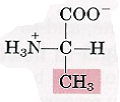 | |
| Valine | 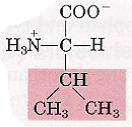 | |
| Leucine | 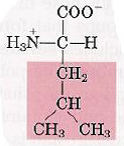 | |
| Isoleucine | 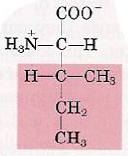 | – Deux carbones asymétriques |
| Méthionine | 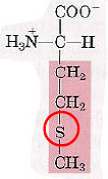 | – Présence d’un atome de soufre – Groupement méthyle CH3 => donneur de méthyle – Intervient donc dans le métabolisme cellulaire (dans le transport de méthyle) |
| Proline | 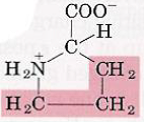 | – La chaîne latérale se cyclise en fonction amine secondaire => Chaîne latérale liée à la fois au carbone α et à l’azote – NH2 dans le cycle = rigidité |
3.4. Propriétés spécifiques des acides aminés apolaires à chaîne aromatique
| Acides aminés | Représentation de leurs états d’ionisation à pH 7.0 | Propriétés spécifiques |
| Phénylalanine | 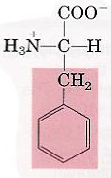 | – Alanine + Cycle phényl – Région polaire et hydrophobe |
| Tryptophane | 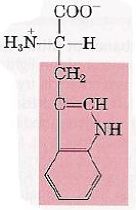 | – Groupe indol – Fort caractère hydrophobe |
Les cycles aromatiques contiennent des électrons π délocalisés qui absorbent fortement dans l’ultraviolet ce qui permet le dosage des protéines en solution : phénylalanine, tryptophane et tyrosine.
3.5. Propriétés spécifiques des acides aminés polaires neutres à fonction alcool
| Acides aminés | Représentation de leurs états d’ionisation à pH 7.0 | Propriétés spécifiques |
| Sérine | 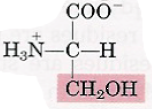 | – Alanine + fonction alcool – La fonction alcool peut fixer un groupement phosphate. => C’est le principe de la phosphorylation (ajout d’un groupement phosphate) des protéines par des protéines kinases en présence d’ATP (transformé en ADP) qui constitue l’un des modes les plus fréquents de la régulation de la fonction d’une protéine. |
| Thréonine | 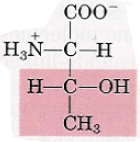 | – La fonction alcool peut fixer un groupement phosphate. – Deux carbones asymétriques |
| Tyrosine | 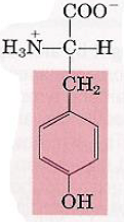 | – Alanine + Cycle phényl + Fonction alcool = phénylalanine hydroxylée (hydrophile) – Point de départ de la synthèse des hormones thyroïdiennes – Régulation de nombreuses protéines – Pas de formation de liaison hydrogène – La fonction alcool peut fixer un groupement phosphate. 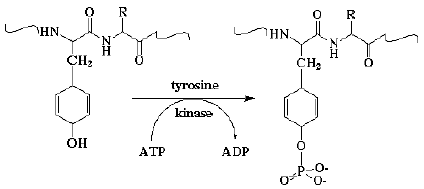 |
3.6. Propriétés spécifiques des acides aminés polaires neutres à fonction soufrée
| Acides aminés | Représentation de leurs états d’ionisation à pH 7.0 | Propriétés spécifiques |
| Cystéine | 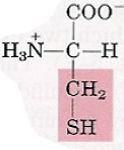 | – Fonction soufrée thiol (-SH) – Deux cystéines peuvent réagir entre-elles par leurs fonctions thiol et former un pont disulfure (S-S). => Réaction d’oxydation pour former un dimère appelé cystine. – Les deux cystéines peuvent être sur la même chaîne protéique (pont intra-chaîne ou intra-caténaire) ou sur deux chaînes différentes (pont inter-chaîne ou inter-caténaire). – Le pont disulfure peut être rompu (réduction) par un agent réducteur comme le β-mercapto-éthanol. 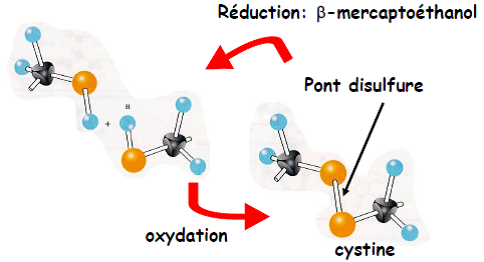 |
3.7. Propriétés spécifiques des acides aminés polaires neutres à fonction amide
| Acides aminés | Représentation de leurs états d’ionisation à pH 7.0 | Propriétés spécifiques |
| Asparagine | 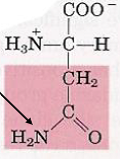 | – Fonction amide CONH2 – Liaison possible à un ose (flèche noire) => Dans les glycoprotéines, les oses se fixent sur l’atome d’azote de la fonction amide de la chaîne latérale de l’asparagine : N-glycosylation |
| Glutamine | 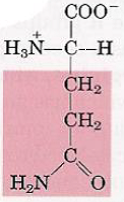 | – Fonction amide CONH2 |
3.8. Propriétés spécifiques des acides aminés polaires ionisables à fonction acide
| Acides aminés | Représentation de leurs états d’ionisation à pH 7.0 | Propriétés spécifiques |
| Acide aspartique | 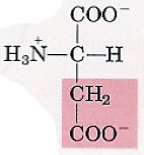 | – pKa(R) = 3,9 – Chargé – à pH 7,0 |
| Acide glutamique | 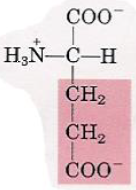 | – pKa(R) = 4,1 – Chargé – à pH 7,0 |
3.9. Propriétés spécifiques des acides aminés polaires ionisables à fonction acide
| Acides aminés | Représentation de leurs états d’ionisation à pH 7.0 (voir fiche de cours « Etats d’équilibre acido-basique ») | Propriétés spécifiques |
| Histidine | 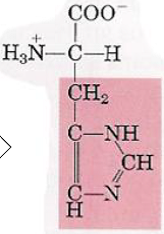 à pH = 5,0 : 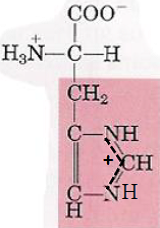 | – pKa(R) = 6,0 – Fonction ionisable – Base faible – Cycle avec deux doubles liaisons – Pas hydrophobe. – Neutre à pH 7,0, Positive à pH 5,0 – Contient un cycle (noyau imidazole) Remarque : l’histidine présente un certain caractère aromatique |
| Lysine | 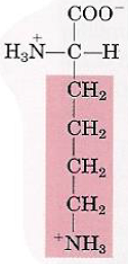 | – Fonction amine – pKa(R) = 10,5 – Chargé + à pH 7,0 |
| Arginine | 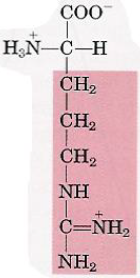 | – Fonction guanidinium – pKa(R) = 12,5 – Chargé + à pH 7,0 |
4. La liaison peptidique
4.1. La liaison peptidique est le ciment de base de toutes les structures protéiques
Liaison peptidique : liaison covalente formée par condensation du groupe α-carboxyle (acide) d’un acide aminé avec le groupe α-aminé d’un autre acide aminé et élimination d’eau.
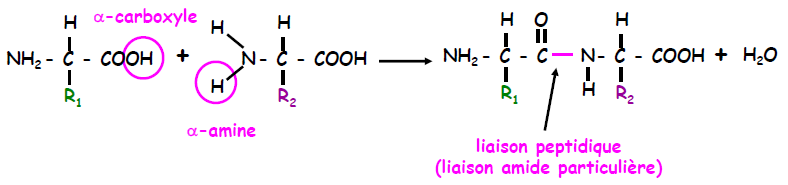
La liaison peptidique est une liaison amide particulière. Elle est un « hybride de résonnance » entre deux formes extrêmes.
| Première forme extrême | Seconde forme extrême | Forme hybride |
| La liaison C O est une double liaison. La liaison C N est une simple liaison. L’azote de l’amide possède une paire d’électrons non partagés. | La liaison C O est une simple liaison. La liaison C N est une double liaison. L’oxygène de l’acide possède une paire d’électrons non partagés. | Les électrons sont partagés entre les atomes O, C et N et sont distribués sur une orbitale moléculaire π qui recouvre les 3 atomes. |
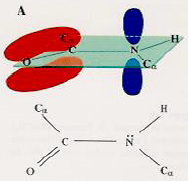 | 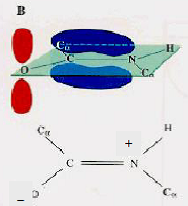 | 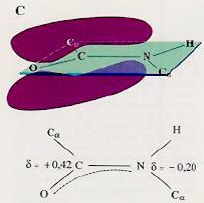 |
En conséquence, la liaison peptidique possède trois propriétés fondamentales. Elle est :
- plane
- rigide
- et polaire.
La liaison peptidique présente des dimensions pratiquement fixes.
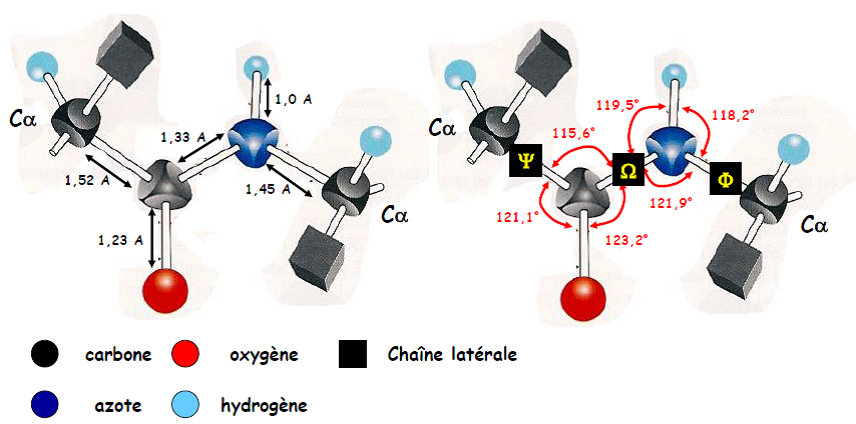
4.2. La liaison peptidique et la nature des résidus amino-acides imposent des structures spatiales très particulières aux chaînes polypeptidiques
Il existe cependant 3 angles qui peuvent prendre des valeurs variables :
| Angles | Caractéristiques |
| Oméga (Ω) | – Angle de torsion autour de la liaison CO-NH – 2 valeurs possibles 0° (CIS) ou 180° (TRANS) 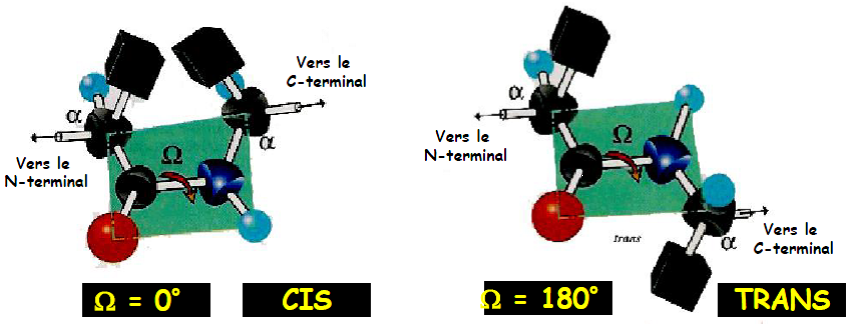 – Configuration TRANS plus stable pour les protéines (les 2 Cα sont de part et d’autre de la liaison) |
| Phi (Φ) et Psi (Ψ) | – Angles de rotation autour de la liaison entre Cα-NH (Φ) et Cα-CO (Ψ) – 2 types de liberté de rotation permettant de modifier la conformation spatiale d’une chaîne polypeptidique 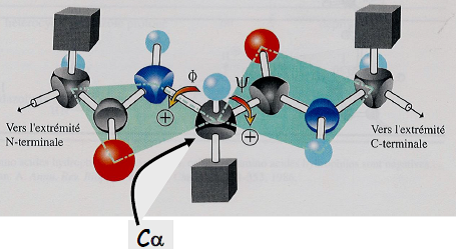 – Fixes pour une structure secondaire donnée (hélices α, feuillets β parallèles, feuillets β antiparallèles… – voir paragraphe 5 sur les « structures secondaires »). 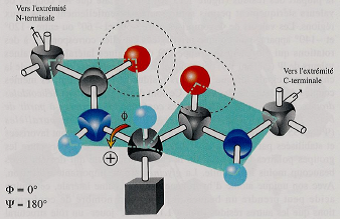 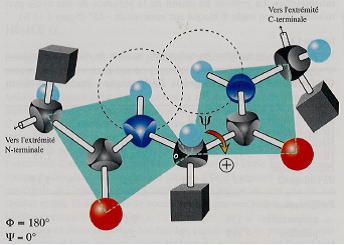 |
4.3. Les chaînes polypeptidiques sont constituées d’un nombre variable de résidus amino-acides et possèdent une structure spatiale spécifique
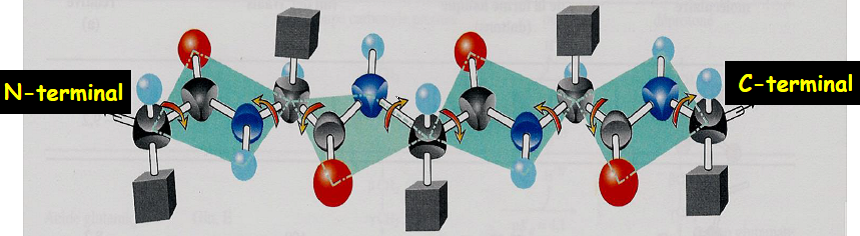
Par définition, une chaîne polypeptidique commence par l’acide aminé qui a sa fonction amine libre (extrémité N-terminale, que l’on place à gauche) et se termine par l’acide aminé qui a sa fonction acide carboxylique libre (extrémité C-terminale placée à droite).
4.4. Groupements chargés dans une chaîne polypeptidique
Ceux sont les charges portées par les chaînes latérales des résidus d’acides aminés qui sont responsables de la charge globale d’une protéine. Elles sont dépendantes du pH.
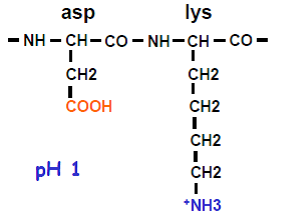 | 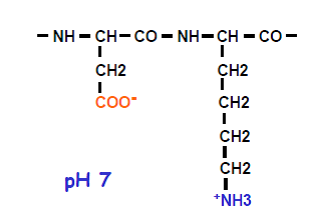 | 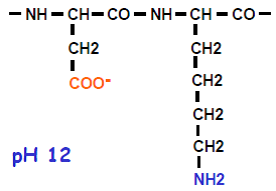 |
La charge globale d’une protéine est majoritairement déterminée par les charges portées par les chaînes latérales des résidus d’acides aminés et est dépendante du pH.
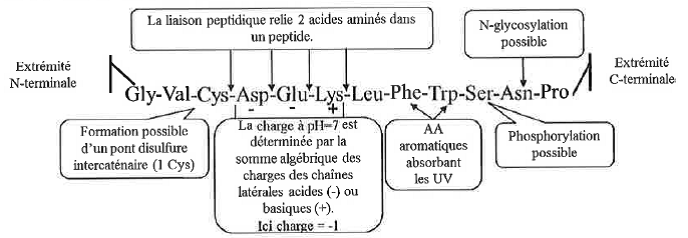
4.5. Les chaînes polypeptidiques peuvent être clivées de façon spécifique
Rupture de la liaison peptidique grâce à des agents biologiques (enzymes protéolytiques = protéases) ou chimiques, possédant chacun une spécificité de coupure :
| Agent | Nature | Spécificité de coupure |
| Trypsine | Enzyme | Après Lysine ou Arginine |
| Chymotrypsine | Enzyme | Après phénylalanine, tyrosine, leucine, tryptophane ou méthionine |
| Bromure de Cyanogène | Produit chimique | Après méthionine |
Exemples :
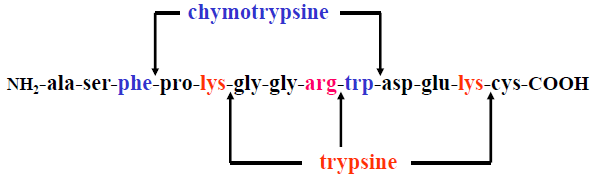
5. Les structures secondaires
5.1. Les différentes structures secondaires
| L’hélice α et les autres hélices | – Structure répétitive et régulière – 13 atomes forment une boucle fermée par une liaison hydrogène entre C=O (accepteur) et H-N (N donneur) des résidus n et n+4 – Valeurs fixées pour les angles Phi (Φ) et Psi (Ψ) : -57° et -47° respectivement – Chaînes latérales des résidus d’acides aminés dirigées vers l’extérieur de l’hélice – Hélice α droite = structure secondaire la plus fréquente 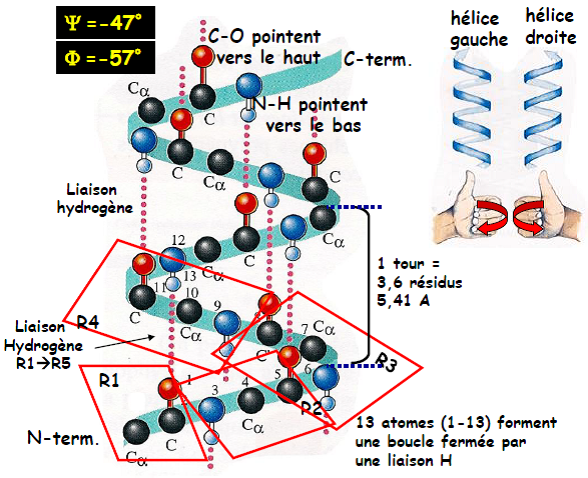 |
| Les feuillets β | – Structure répétitive et régulière – Formation de liaisons hydrogènes entre plusieurs brins pour former un feuillet – Structure plane, ondulée avec les chaînes latérales des résidus d’acides aminés dirigées au-dessus ou en-dessous du plan du feuillet – 2 types de feuillet bêta : antiparallèle et parallèle (en fonction de l’orientation des brins) – Antiparallèle est plus stable donc plus fréquent au sein des protéines – Valeurs fixées pour les angles Phi (Φ) et Psi (Ψ) mais différentes pour un feuillet β parallèle (-119°, +113°) et un feuillet β antiparallèle (-139°, +135°) 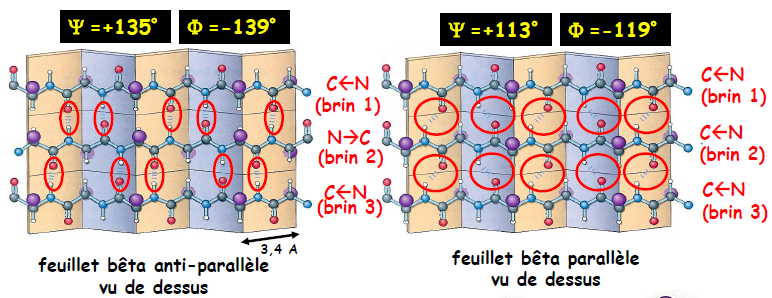 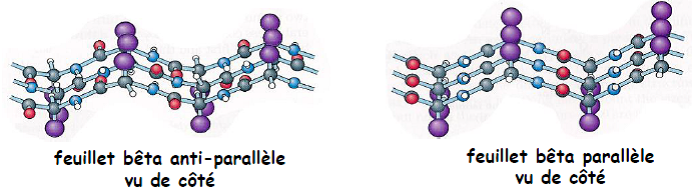 |
| Coudes et boucles | – Structures non régulières, non répétitives – Permettent la connexion entre structures secondaires régulières – Les coudes ne possèdent que quelques résidus, par exemple 4 résidus dans certains coudes, stabilisés par une liaison hydrogène Exemple de coude β (type I) 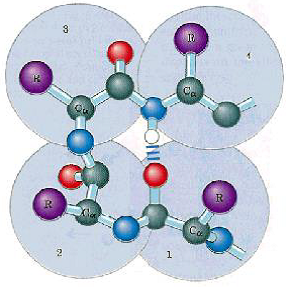 – Les boucles peuvent atteindre une vingtaine de résidus et se trouvent souvent à l’extérieur des protéines pour former des liaisons hydrogène avec l’eau du milieu. 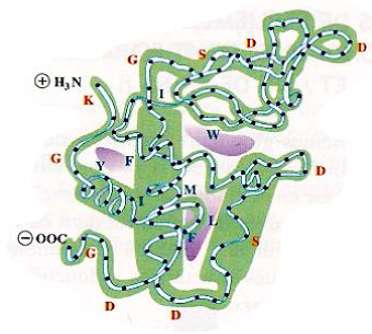 |
5.2. Prédiction de structure et bioinformatique
Ces propriétés spécifiques font que chaque acide aminé préfère un environnement conformationnel donné. Les nouveaux outils bioinformatiques permettent de faire des prédictions.
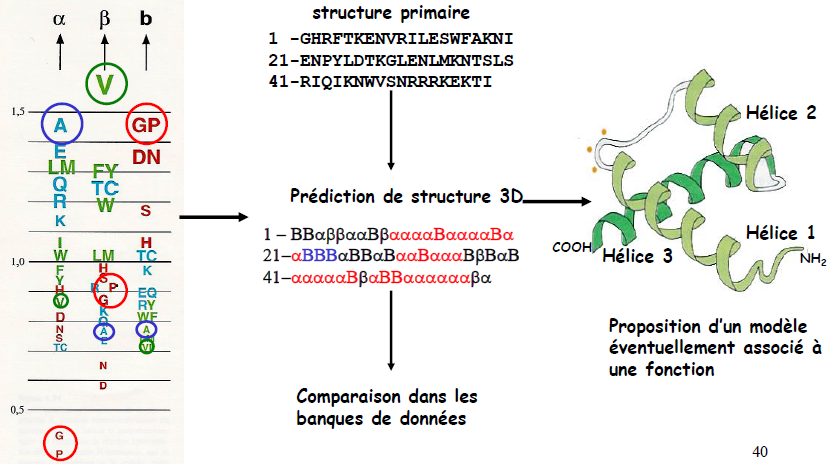
Ainsi, certains acides aminés se retrouvent préférentiellement dans certaines structures, ou au contraire certains acides aminés empêchent la formation d’une structure secondaire :
| Hélices α | Feuillets β | Coudes | |
| Acides aminés présents | Alanine | Valine | Glycine, Proline |
| Acides aminés déstabilisant | Glycine, Proline | Glycine, Proline, Alanine | Alanine, Valine |
6. La notion de motif et de domaine
On trouve dans les protéines des combinaisons de structures secondaires. Ces combinaisons s’appellent des « motifs » et des « domaines ». Ils peuvent se retrouver dans des protéines différentes. Ils apportent à ces protéines une fonction commune.
Exemples :
| « hélice-coude-hélice » | – Correspond à un motif composé d’une hélice α séparée d’une autre hélice α par un coude. – Est présent dans beaucoup de protéines se fixant à l’ADN. | 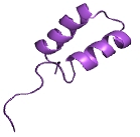 |
| Motif ou domaine immunoglobulinique | – est l’élément constitutif des immunoglobulines – Correspond à une structure globulaire compacte constituée de feuillets bêta | 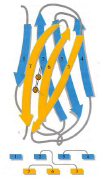 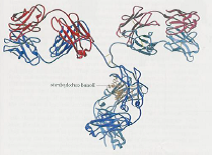 |
7. Structures primaire, secondaire, tertiaire et quaternaire
- La séquence des acides aminés (structure primaire) détermine la structure tridimensionnelle.
- Une structure primaire donnée conduit à une structure tridimensionnelle donnée.
- La séquence des acides aminés (structure primaire) est déterminée par le gène.
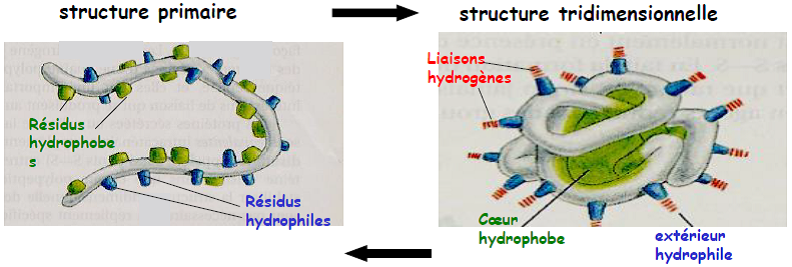
La dénaturation correspond à une perte de l’activité. Elle peut s’opérer grâce à des agents dénaturants comme l’Urée 8M et le chlorure de guanidine qui rompent les liaisons non covalentes.
Les protéines peuvent présenter jusqu’à 4 types de structures :
- Structure primaire : séquence (ou enchaînement) des acides aminés d’une protéine
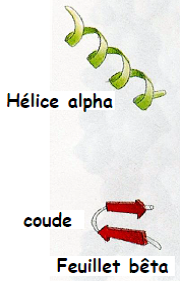
- Structure secondaire : motifs structuraux de base (hélice α, feuillet β, coude…)
- Structure tertiaire : organisation interne d’une protéine (ou d’une sous-unité)
- Structure quaternaire : organisation complexe d’une protéine multi-mérique (au moins dimérique)
| Structure secondaire | Structure tertiaire | Structure quaternaire |
 | 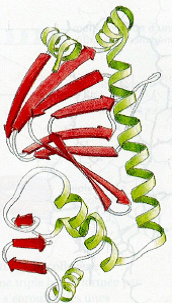 | 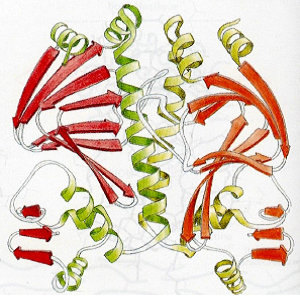 |
8. Structure et pathologie… le mystère de la vache folle !
La modification de la structure d’une protéine particulière, le prion, peut lui conférer un rôle pathologique.
Existence de 2 structures tridimensionnelles différentes pour une seule et même structure primaire :
- Protéine prion normale = PrPc
- Protéine prion infectieuse « scrapie » = PrPsc (moins d’hélices α mais plus de feuillets β)
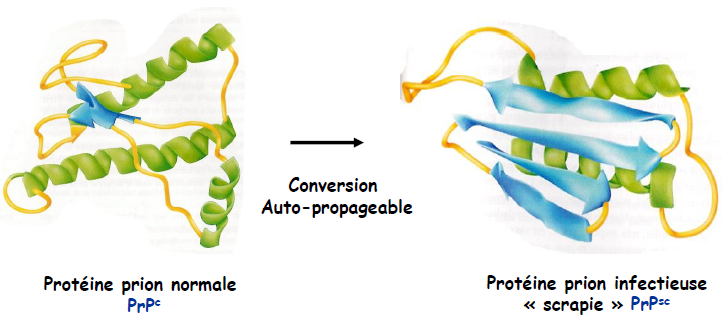
Conversion entre les 2 protéines auto-propageable : la PrPsc infectieuse induit la transformation de PrPc normale en PrPsc infectieuse.
