Cytosquelette
Ce que vous savez du lycée
| De la seconde* : | / |
| De la première** : | / |
| De la terminale*** : | / |
**adapté du programme officiel de Sciences de la Vie et de la Terre de première générale publié au Bulletin Officiel de l’Education Nationale.
***adapté du programme officiel de spécialité de Sciences de la Vie et de la Terre de terminale générale publié au Bulletin Officiel de l’Education Nationale.
1. Présentation
1.1. Constituants
| Microtubules | Microfilaments | Filaments intermédiaires | |
| Le cytosquelette est composé de trois types principaux de filaments de diamètres différents : | 25 nm | 8 nm | 10 nm |
| Chaque type de filament est composé par l’assemblage de monomères spécifiques. | Tubuline | Actine | Kératines, vimentine… |
| La distribution spatiale et l’organisation de chaque type de réseau de filaments est particulière. |  | 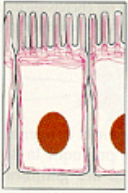 |  |
De très nombreuses protéines sont associées à ces filaments. Elles orientent et contrôlent les fonctions du cytosquelette (voir plus loin).
1.2. Fonctions
Le cytosquelette assure principalement deux types de fonctions :
- Il permet le maintien ou l’adaptation à l’environnement de la structure cellulaire et le positionnement des organites intracellulaires.
- Il supporte les fonctions motrices de la cellule :
- déplacement des organites et des vésicules (= trafic intracellulaire),
- déplacement cellulaire (= motilité).
La contribution du cytosquelette à ces fonctions dépend fortement du type de filament et des protéines qui lui sont associées.
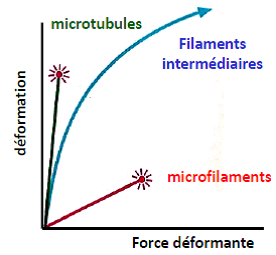
Chaque type de filament a des propriétés spécifiques de résistance à la déformation.
Les différents types de filaments s’associent ou se relayent souvent pour assurer les fonctions du cytosquelette.
2. Les filaments intermédiaires
2.1. Structure & assemblage
Les filaments intermédiaires sont des structures fibreuses, compactes et résistantes, formées par l’association complexe de nombreux monomères.
Un monomère de filament intermédiaire est formé d’une région centrale très riche en hélices α, conférant une structure en bâtonnet.
Cette région est également riche en répétition heptade (coil-coil) favorisant les interactions protéine-protéine.
| Monomère |  |
| Dimère super-enroulé |  |
| Tétramère (2 dimères étagés) |  |
| Deux tétramères super-enroulés | |
| Un filament intermédiaire de base | 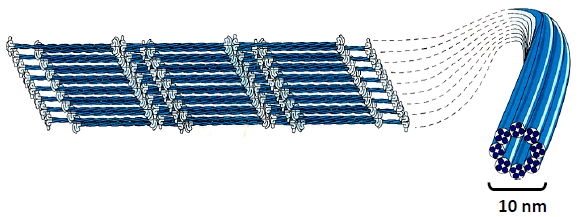 |
2.2. Diversité
Il existe une grande diversité de monomères de filaments intermédiaires. Ils sont à l’origine de filaments dont la localisation et la fonction sont différentes.
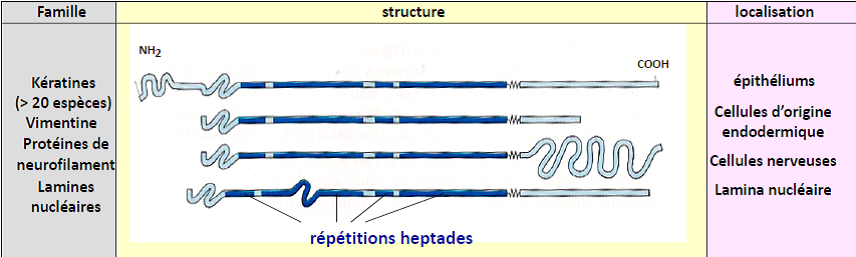
2.3. Fonctions
Les fonctions des filaments intermédiaires concernent principalement le maintien de l’architecture cellulaire et tissulaire. Elles dépendent essentiellement du type de filament.
| Dans les épithéliums, les kératines relient les cellules entre elles par l’intermédiaire des desmosomes. Les kératines assurent la cohésion et la stabilité mécanique. | Exemple de pathologie : l’épidermolyse bulleuse => mutation sur une kératine, => cisaillement cellulaire au niveau des kératines défectueuses. | 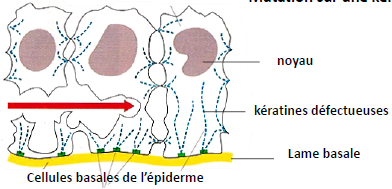 |
Dans les cellules nerveuses, les neurofilaments assurent la continuité et l’élasticité des neurones.
| Dans les noyaux, les lamines assurent la stabilisation de la membrane nucléaire interne et l’interaction avec la chromatine. | 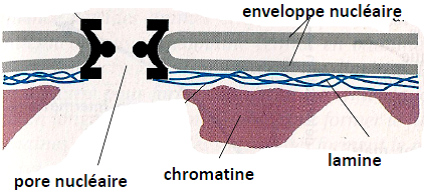 |
3. Les microtubules
3.1. Structure & assemblage
| Un microtubule est un assemblage de deux types de monomères très semblables : tubuline α et β. La tubuline β contient un GTP échangeable. Dimère => protofilament => tube creux. |  |
| La formation d’un microtubule comprend trois phases : | 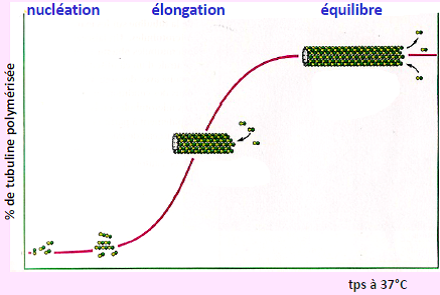 |
| L’assemblage est en fait la résultante d’un équilibre entre polymérisation et dépolymérisation. | 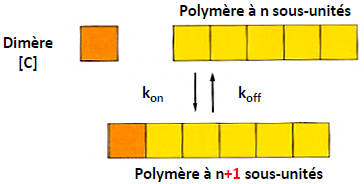 |
| Il existe une concentration critique en dimères : Cc, pour laquelle le gain et la perte de sous-unités s’équilibrent. |  |
L’assemblage est asymétrique : il existe une extrémité plus à croissance rapide et une extrémité moins à croissance lente.
in vitro : incubation avec tubuline α et β, GTP et facteurs de polymérisation.
L’asymétrie des microtubules est retrouvée in vivo dans tous les types cellulaires et dans toutes les situations.
| L’asymétrie de croissance des microtubules est liée à des changements conformationnels des sous-unités lorsqu’elles entrent dans le polymère. Une hydrolyse du GTP en GDP intervient peu de temps après l’association du dimère au polymère (le GTP est un nucléotide similaire à l’ATP). | 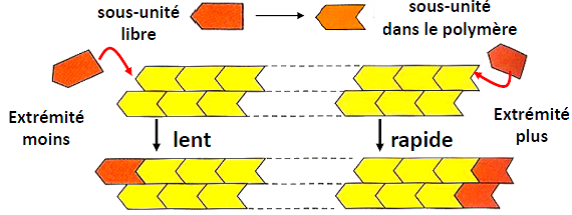 |
| La forme D a moins d’affinité pour le polymère et tend à se dissocier. C’est donc la concentration en forme T libre (dimère GTP) qui est critique pour l’élongation. Si cette concentration est suffisante (C >> Cc) l’élongation est plus rapide que l’hydrolyse et le microtubule croît. |  |
3.2. Un exemple de l’instabilité dynamique des microtubules
L’équilibre croissance-dépolymérisation est dynamique et repose sur des mécanismes complexes de phosphorylation/déphosphorylation du couple GTP/GDP.
| L’élongation à l’extrémité moins est lente. Les dimères sont hydrolysés sous forme D et ont tendance à se dissocier. L’élongation à l’extrémité plus est rapide. Les dimères sous forme T qui polymérisent n’ont pas le temps d’être hydrolysés. | 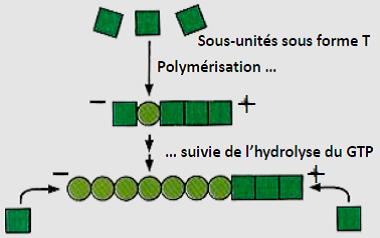 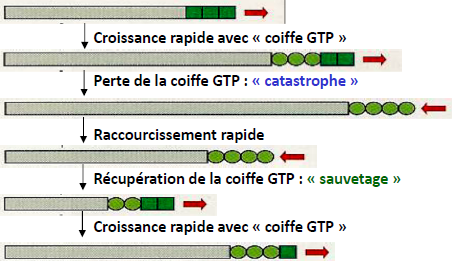 |
| L’équilibre croissance-dépolymérisation est dynamique et repose sur des mécanismes complexes de phosphorylation/déphosphorylation du couple GTP/GDP. | 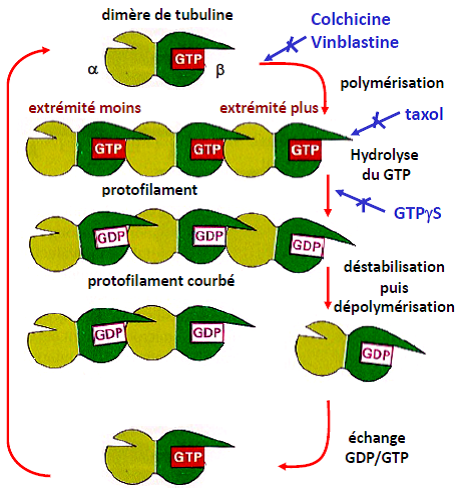 |
Des modifications post-traductionnelles (acétylation, détyrosination, polyglutamination) peuvent moduler la stabilité des microtubules.
3.3. Deux types de protéines associées aux microtubules
| Protéines régulatrices exemples : MAP-2, tau. | Elles ont plusieurs fonctions : – Stabilisation des extrémités des microtubules (favorisent la nucléation, empêchent la dépolymérisation). – Formation de liaisons entre plusieurs microtubules. – Interactions avec divers composants cellulaires. |
| Protéines motrices exemples : kinésines et dynéines. | = Moteurs moléculaires. Le déplacement des moteurs moléculaires kinésines et dynéines dépend de la production d’énergie par un domaine ATPasique. 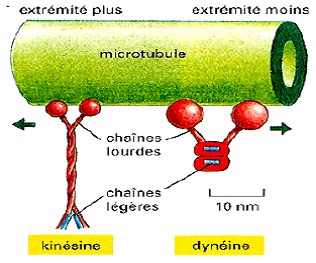 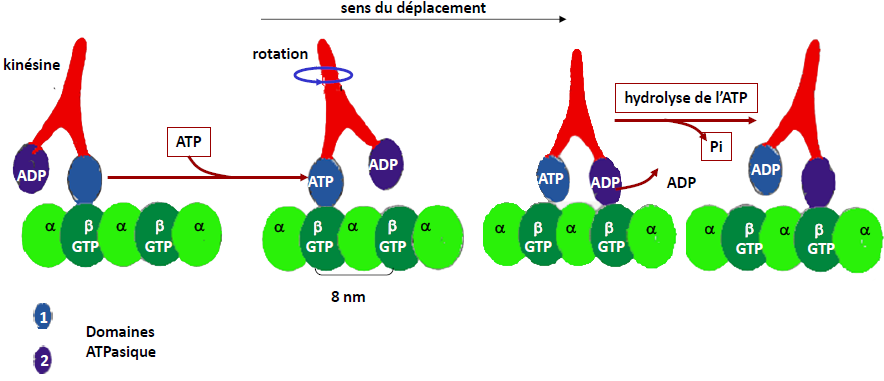 |
3.4. Fonctions du réseau de microtubules
| Fonctions de transport | La plupart des étapes du trafic intracellulaire (exocytose/endocytose) utilise les microtubules et les moteurs moléculaires pour assurer le trafic antérograde (kinésines) et le trafic rétrograde (dynéines). Les microtubules transportent : – des vésicules, – les complexes chromosomes/protéines associées, lors de la mitose, – des ARNm vers leur lieu d’utilisation (exemple du « patterning » antéro-postérieur chez la drosophile), – des virus (HIV, herpès…) de la membrane cellulaire vers le lieu de réplication. Ces différents « chargements » sont pris en charge par des moteurs moléculaires distincts. 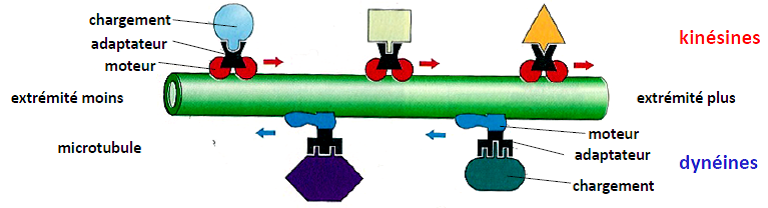 |
| Fonctions d’organisation du cytosol et des compartiments membranaires | Le centrosome : – Est le principal centre organisateur du cytosol. – Supporte l’asymétrie des microtubules. – Est un centre nucléateur. – Est composé de deux centrioles et d’une matrice. 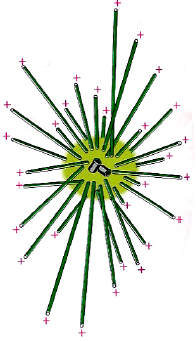 L’extrémité moins des microtubules est enchâssée dans le centrosome. Les microtubules enchâssés dans le centrosome ont une grande dynamique. Cette dynamique assure le positionnement dynamique des organites intracellulaires. 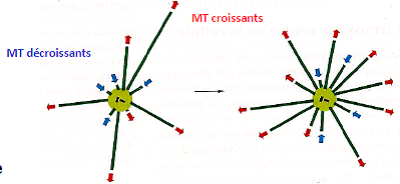 |
| Cils et flagelles : formes spécialisées des réseaux de microtubules | Structures apparentées dans lesquelles les microtubules sont organisés en axonème. => deux types d’axonèmes : 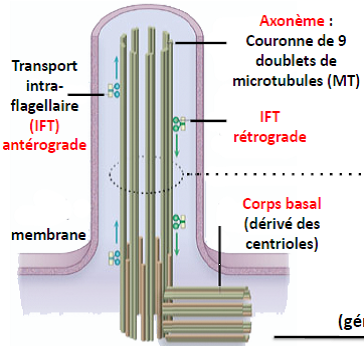 Cils primaires – Généralement immobiles. – Présents dans toutes les cellules eucaryotes. – Fonctions de signalisation +++. – Impliqués dans les ciliopathies (ex : polykystoses, anomalies de développement embryonnaires, diabète, obésité…). 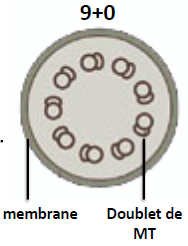 Cils secondaires et flagelles – Mobiles, vibratiles. – Présents dans certaines cellules procayotes et eucaryotes. – Mouvement de battement (cils) ou de propulsion (flagelles). – Impliqués dans des pathologies (ex : pathologies respiratoires, stérilité…). 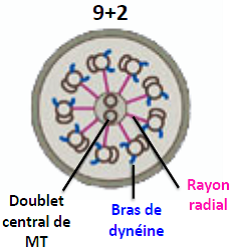 |
4. Les microfilaments
4.1. Structure et assemblage
| L’assemblage des filaments d’actine est similaire à celui des microtubules. L’assemblage (polymérisation) est réalisé par addition de monomères aux deux extrémités. L’addition est plus rapide à l’extrémité plus et plus lente à l’extrémité moins. | 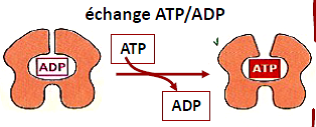 |
| Les cytochalasines, en se fixant sur l’extrémité plus, bloquent la polymérisation des microfilaments. Les phalloïdines (de l’amanite phalloïde), en se fixant sur les microfilaments, bloquent leur dépolymérisation. | 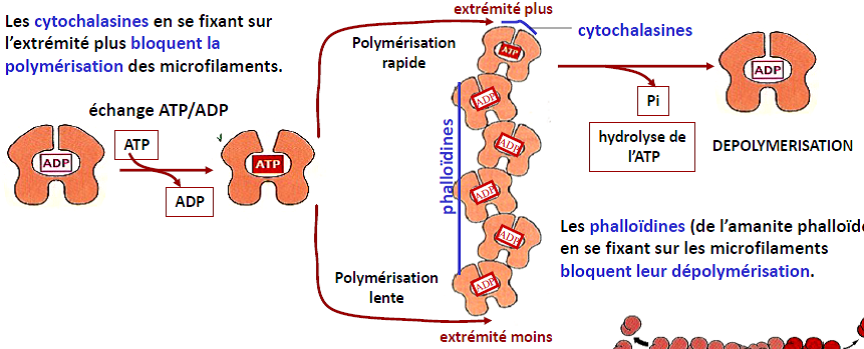 |
Lorsque les 2 extrémités sont libres et que les conditions de concentration intracellulaire de monomères sont favorables, l’association et la dissociation aux deux extrémités plus et moins se fait à la même vitesse. Dans ce cas particulier, la longueur du filament reste constante mais le filament se déplace en glissant (« treadmilling »).
4.2. Protéines de liaison à l’actine
1- Participant à l’organisation des MF
| fimbrine, villine | Formation de faisceaux serrés de MF. |
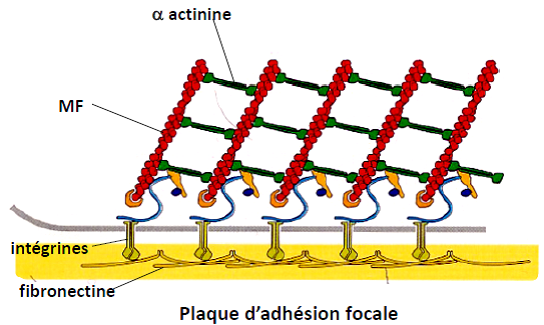
| α-actinine | Formation de faisceaux larges de MF. |
| filamine | Formation d’une réticulation de MF. |
| spectrine, dystrophine | Ancrage à la membrane. |
2- Participant aux fonctions motrices des MF
| myosine II | Effectue la contraction musculaire en déplaçant les microfilaments. |
| myosines I, V (etc…) | Assurent les mouvements le long des microfilaments. |
| tropomyosine | Stabilise les microfilaments. |
3- Participant à la dynamique des MF
| profiline, ARP 2/3 | Favorisent la polymérisation des MF. |
| thymosine, ADF/cofiline, gelsoline | Favorisent la dépolymérisation et/ou coupent les MF. |

4.3. Fonctions du réseau de microfilaments
1- Création, maintien et dynamique de structures cellulaires
Cortex cellulaire
Le réseau de MF s’organise sous la membrane plasmique et permet le déplacement cellulaire.
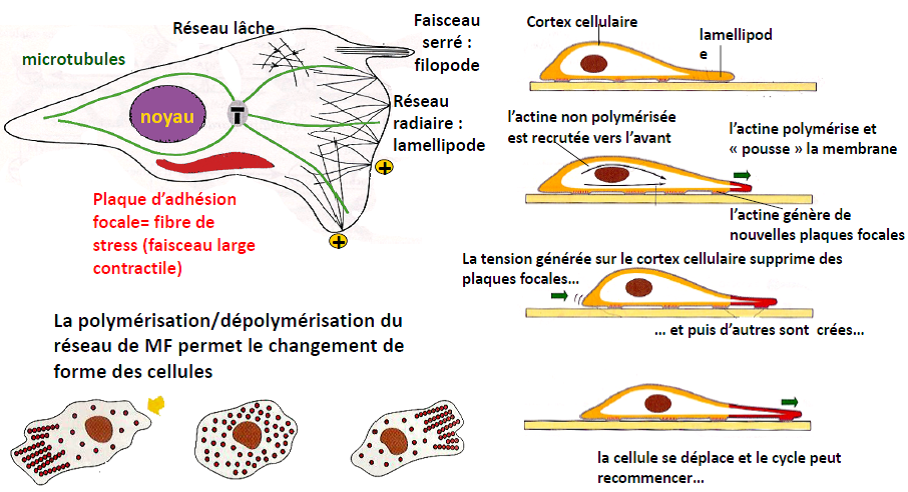
Les fonctions du réseau de microfilaments sont étroitement dépendantes des protéines associées.
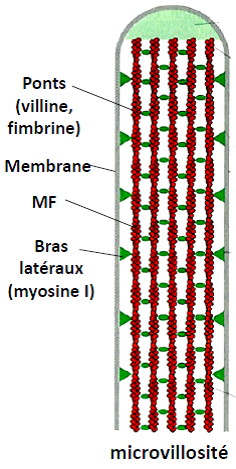
| Microvilli | Epithélium |
| Stéréocils | Oreille interne |
| Filopode | Cellules en migration |
| Lamellipode | Cellules en migration |
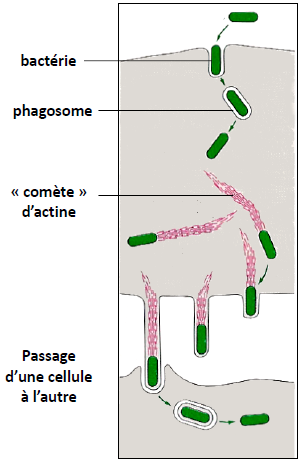
2- Fonctions motrices
Certaines bactéries recrutent l’actine cellulaire pour se propulser dans la cellule et pour passer d’une cellule à l’autre.